Eutektik
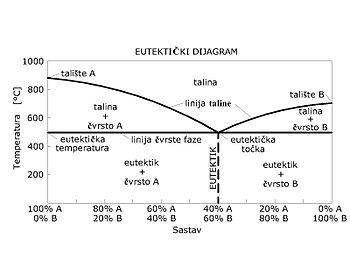

Eutektik ili eutektička mješavina je kruta otopina sastavljena od dviju ili više tvari koja ima niže talište od svake čiste komponente ili bilo koje njihove smjese (legura). Eutektička točka je najniža temperatura na kojoj eutektična smjesa može postojati u tekućoj fazi, i u njoj je jednak sastav tekuće i krute faze. Eutektik se javlja kod dva metala koji se potpuno miješaju u tekućem, a ne miješaju se u čvrstom stanju. Eutektička legura se skrućuje kod konstantne temperature, pa je njezina krivulja hlađenja ista kao i za čiste metale.[1]
Kod eutektičke mješavine kristalizacija se vrši naizmjenično tj. čisti metal A, pa metal B itd., što rezultira s finom mješavinom lamelarnih (listići) kristala A i B, poznatih pod nazivom eutektička mješavina ili eutektik. Temperatura ostaje nepromijenjena sve dok se ne skrutne čitava talina. Eutektička reakcija je promjena taline u dvije čvrste faze prilikom hlađenja, te obratno kod zagrijavanja:
- talina ⇔ čvrsto A + čvrsto B
Eutektoid[uredi | uredi kôd]
Eutektoidna reakcija je veoma je slična eutektičkoj reakciji. Eutektoidna mješavina ili eutektoid ima finu lamelarnu (listići) strukturu donekle sličnu eutektičkoj mješavina, pa se ove dvije strukture teško mogu razlikovati optičkim mikroskopom.[2]
- čvrsto α ⇔ čvrsto A + čvrsto B
Peritektik[uredi | uredi kôd]
U peritektičnoj reakciji talina i jedna čvrsta faza reagiraju izotermički, pri čemu nastaje druga čvrsta faza. Nova faza obično je terminalna (rubna, marginalna) čvrsta otopina ili intermetalna faza.
- talina + čvrsto α ⇔ čvrsto β
Peritektoid[uredi | uredi kôd]
Peritektoidna reakcija je reakcija u čvrstom stanju, koja se javlja rjeđe od eutektoidne reakcije:[3]
- čvrsto α +čvrsto ß ⇔ čvrsto γ
Djelomično miješanje u tekućem stanju[uredi | uredi kôd]
Kod djelomičnog miješanja u tekućem stanju nastaje:
- monotektična reakcija: talina 1 → čvrsto α + talina 2
- sintektična reakcija: talina 1 + talina 2 → čvrsto γ .
Izvori[uredi | uredi kôd]
- ↑ [1] Arhivirana inačica izvorne stranice od 4. srpnja 2014. (Wayback Machine) "Fizikalna metalurgija I", dr.sc. Tanja Matković, dr.sc. Prosper Matković, www.simet.unizg.hr, 2011.
- ↑ [2] Arhivirana inačica izvorne stranice od 31. srpnja 2013. (Wayback Machine) "Metali", www.ffri.uniri.hr, 2011.
- ↑ "Strojarski priručnik", Bojan Kraut, Tehnička knjiga Zagreb 2009.
