Gorivi članak
Gorivni članak je elektrokemijski uređaj koji služi za neposrednu pretvorbu kemijske energije, sadržane u nekom kemijskom elementu ili spoju, u istosmjernu električnu struju. Gorivni se članak, isto tako kao i baterija, sastoji od dviju elektroda uronjenih u isti elektrolit. Na anodi gorivnog članka oksidira gorivo, tj. neki kemijski element ili spoj visokog sadržaja unutarnje energije. Elektroni, proizvedeni oksidacijom goriva, odvode se od anode vanjskim krugom vodiča i preko trošila (otpornik, električni motor istosmjerne struje, žarulja i sl.) do katode. Na katodi neki se drugi element ili spoj (oksidans) reducira zahvatom elektrona proizvedenih na anodi. Proizvodi reakcije, negativni i pozitivni ioni, spajaju se u elektrolitu, a nastali produkt odvodi se iz gorivnog članka. Često je konačni produkt reakcije isti kao da je gorivo izgorjelo u oksidansu uz izravnu pretvorbu kemijske u unutrašnju toplinsku energiju. Odatle i potječe naziv gorivni članak.
Gorivni članci su visoko djelotvorni pretvarači energije. Bez pokretnih su dijelova i rade bez buke. Primjena gorivnih članaka ograničena je za sada na svemirske letjelice i u neke vojne svrhe, dakle tamo gdje visoka nabavna cijena nije problem.

Povijest gorivnog članka[uredi | uredi kôd]
Gorivni članak otkrio je William Robert Grove 1839. godine opažanjem da se obratom elektrolize vode, tj. dovođenjem vodika na jednu i kisika na drugu elektrodu može dobiti električna struja. Svoje pokuse opisao je 1842. kada govori o plinskoj voltinoj bateriji. Grove je prvi opazio da se električna energija stvara na mjestu dodira triju faza: plinske (vodik ili kisik), tekuće (vodljivi elektrolit) i čvrste (platinska elektroda). Opazio je također da jakost struje određuje aktivna površina elektrode, te je stoga počeo eksperimentirati sa spužvastom platinom, poroznim metalom velike specifične površine. Tako je ne samo otkrio gorivni članak, nego zacrtao i problematiku istraživanja za više od jednog stoljeća. Groveova zapažanja obnovili su tek 1889. godine Ludwig Mond i Carl Langer. Oni su gorivnom članku vodik - kisik dodali separator, poroznu, vodljivu membranu za odvajanje anodnog i katodnog prostora, smanjujući mu na taj način dimenzije. Krajem XIX. stoljeća W. Ostwald i W. Nernst upozorili su na termodinamičke osnove pretvorbe energije i definirali termin gorivnog članka. Iz tog doba poznati su pokušaji W. W. Jaquesa da kemijsku energiju ugljena iskoristi u gorivnom članku. Iako su na razvoju gorivnih članaka teorijski i eksperimentalno radili mnogi istaknuti kemičari i elektrokemičari (uz već spomenute još i Fritz Haber, Karl A. Hofmann i Erwin Baur), suvremena, tehnički primjenjiva rješenja počinju tek radom engleskog istraživača F. T. Bacona 1932. godine. Sredinom 50–ih godina ostvarene su prve gorivne članke pogodne za pogon prijevoznih sredstava i manjih električnih uređaja. Osobiti poticaj razvoju gorivnih članaka dali su programi istraživanja svemira u SAD i SSSR. Sredinom 60-ih godina 20. stoljeća glavni sustavi napajanja svemirskih letjelica električnom energijom bili su zasnovani na gorivnim člancima tipa vodik-kisik s platinskim elektrodama i ionsko-izmjenjivačkim membranama kao nosačem elektrolita. Zbog nedovoljnog poznavanja osnova kinetike i mehanizama elementarnih elektrokemijskih procesa, istraživanja su sporo napredovala i nije bilo uspješnih ekonomičnih i tehničkih rješenja gorivnih članaka. Spoznaje o materijalima i njihovim površinskim svojstvima, o zakonitostima prijenosa mase i naboja preko granica faza i o strukturi elektrokemijskog dvosloja rezultat su istraživanja 50-ih i 60-ih g.
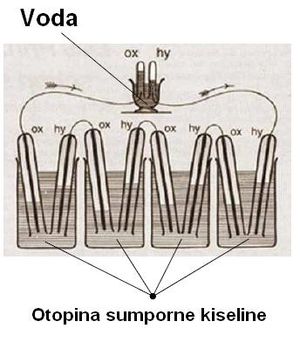
Princip rada gorivnog članka[uredi | uredi kôd]
Princip rada[uredi | uredi kôd]
Princip rada gorivnog članka može se najlakše objasniti na do sada najbolje razvijenom sustavu s vodikom kao gorivom i kisikom kao oksidansom. Kada se vodik i kisik u plinskom stanju dovedu u kontakt i aktiviraju, oni reagiraju, spajaju se u vodu i oslobađaju energiju: 2H2 + O2 › 2H2O + energija.
U gorivnom članku ta se ukupna reakcija sastoji od dviju reakcija, od kojih svaka teče na jednoj elektrodi. Na anodi se oksidira vodik i oslobađaju se elektroni: H2 › 2H+ + 2e. Elektroni se vode kroz vanjske vodiče preko trošila na katodu, gdje se reducira kisik: O2 + 2H2O + 4e › 4OH-.
Redukcija kisika je složena, višestruka reakcija, čiji mehanizam ovisi i o naravi elektrodne površine. Ukupna reakcija sastavljena je od nekoliko podreakcija: O2 › O + O (disocijacija), u kojoj se atomski kisik adsorbira na površini metalne elektrode. Reakcija s vodom: O + H2O › 2OH (hidroksilacija). Nastaju hidroksilne skupine, adsorbirane kao hidroksid na površini metala, koje se konačno reduciraju u ione OH + e › OH-(elektonacija, redukcija).
U gorivnom članku s kiselim elektrolitom vodikovi ioni, stvoreni na anodi, putuju kroz elektrolit i spajaju se u reakcijskom sloju katode s hidroksilnim ionima u vodu. U članku s alkalnim elektrolitom hidroksilni ioni dolaze difuzijom kroz elektrolit u reakcijski sloj anode, gdje se s vodikovim ionima rekombiniraju u vodu. Spomenuti slijed reakcija jest tzv. oksidni put redukcije kisika. Postoji još čitav niz drugih mehanizama prema kojima se u gorivnim člancima reducira oksidans, a oksidiraju različite molekule koje služe kao gorivo. Spomenuti primjer pokazuje složenost elektrokemijskih reakcija i probleme s kojima se suočavaju konstruktori gorivnih članaka. Radi ubrzavanja reakcija elektrode su prekrivene slojem katalizatora. Vrsta katalizatora ovisi o tipu gorivnog članka.
Dijelovi i reagensi gorivnih članaka[uredi | uredi kôd]
Dijelovi i reagensi gorivnih članaka su elektrode, katalizatori, elektroliti, goriva i oksidansi.
Elektrode[uredi | uredi kôd]
Na elektrodama gorivnog članka odvijaju se elektrokemijske reakcije oksidacije i redukcije. Elektrode imaju višestruku funkciju. One provode elektrone, pa se izrađuju iz metala ili materijala s poluvodičkim svojstvima. Površina elektrode mora katalizirati elektrokemijsku reakciju adsorbiranjem i disociranjem reaktanata, te brzim desorbiranjem proizvoda reakcije. Od elektrode se traže dobra mehanička svojstva, tako da se mogu izraditi u željenom obliku, s visokom specifičnom površinom i određenom veličinom pora. Elektrode ne smiju korodirati u elektrolitu gorivnog članka, ali su štetni i zaštitni oksidni slojevi, koji pružaju otpor prolazu elektrona. Svim tim zahtjevima odgovaraju samo neki metali: platina, paladij, rodij, rutenij, te do neke mjere nikal za anode i srebro za katode. Grafit je također dobar materijal za elektrode u gorivnim člancima koje rade pri srednjim ili visokim temperaturama.
Plemeniti metali su skupi i nema ih dovoljno. Za neke od suvremenih elektroda upotrebljavaju plemenite metale u obliku finih disperzija u matrici nekog polimera (teflon, polietilen) na nosaču od nikla, bakra ili nekog drugog neplemenitog metala. Za takve elektrode s platinom potrebno je 1…20 mg platine za cm2 aktivne površine i oko 20 mg za svaki Vat snage. Tipične su gustoće struje 0,5 A/cm2 uz napon na stezaljkama 0,6….0,9 V. Široka primjena gorivnih članaka u budućnosti ovisi o pronalaženju drugih, jeftinijih materijala za elektrode.
Rad gorivnih članaka s plinovitim reaktantima ovisi o transportu materije i prijenosu naboja na granici triju faza: plinovito - tekuće - čvrsto. Pri tome je najvažnija poroznost elektroda. Plin ulazi u pore elektroda i mora dospjeti do onog dijela koji je natopljen elektrolitom. Plin se tada ionizira, a elektrolit prihvaća i odvodi nastale ione. Znatna gustoća struje i dovoljan transport materije može se ostvariti samo na mjestu, gdje je put difuzije plina kroz tekućinu kratak, a debljina sloja tekućine ipak tolika da je odvod produkata reakcije dovoljno intenzivan. To se mjesto naziva područjem reakcije. Proračun promjera pora, tlaka ulaznog plina, te stanje površine elektroda kritični su elementi tehnologije elektroda gorivnog članka.
Tlak plina određuje položaj meniska u porama. Potapanje pora elektrolitom zbog premalog tlaka plina ili istiskivanje elektrolita iz pora prevelikim tlakom obustavlja elektrokemijsku reakciju u porama, a na taj način i rad gorivnog članka. Najboljim su se pokazale elektrode s različitim veličinama pora. U takvim su elektrodama pore na strani elektrolita uske, pa imaju veliki kapilarni učinak. Na strani plina pore su široke, te plin u njih lako ulazi. Na taj način položaj meniska, koji se uspostavlja na granici između uskih i širokih pora, može bolje regulirati i nije toliko ovisan o tlaku plina. Karakteristični promjeri uskih i širokih pora u gorivnom članku tipa vodik – kisik iznose 10….15 µm, odnosno 30….50 µm. U proizvodnji tih elektroda upotrebljavaju se dvije vrste monodisperzivnih metalnih praškova. Sloj velikih čestica postupno se sinterira na već formiranu podlogu s manjim česticama.
Katalizatori[uredi | uredi kôd]
Tok elektrokemijske reakcije i gustoća struje ovise o katalitičkim pojavama na površini elektroda. Elektroda može biti ujedno i katalizator (elektrokatalizator), ako se određenim postupkom obradi ili ako se na njenu površinu katalizator adsorbira. Izbor katalizatora ovisi o najsporijem elementarnom stupnju ukupne reakcije, koji treba ubrzati ili mu smanjiti otpor.
Elektroliti[uredi | uredi kôd]
U elektrolitu se prenosi naboj difuzijom iona s jedne na drugu elektrodu. Upotrebljavaju se tekući i čvrsti elektroliti. Svaka polarna tekućina, koja otapa ionske kristale, može biti tekući elektrolit. To mogu biti i rastaljene soli, ponajviše one alkalijskih metala (kloridi i karbonati). Od čvrstih elektrolita važni su ionski izmjenjivači, membrane građene od polimera (npr. polistirena) s aktivnim skupinama SO3H, COOH, OH ili NH2. Takve membrane odvajaju katodni od anodnog prostora, te smanjuju dimenzije gorivnog članka. Djelovanje gorivnog članka s čvrstim elektrolitom ne ovisi o gravitaciji, te se oni stoga primjenjuju u svemirskim letjelicama. Visokotemperaturni gorivni članci sadrže čvrste elektrolite (Al2O3, ZrO2 i MgO), koji su dopirani (kontrolirano onečišćeni) dodatkom metala (iona iz grupe alkalija, zemnoalkalija ili lantanida). U novije doba ispituju se elektrolitički vodljive membrane od niklovog borida i borovog nitrida.
Goriva[uredi | uredi kôd]
Svaki kemijski element ili spoj visokog sadržaja unutrašnje energije, koji tu energiju može oksidacijom osloboditi i prijeći u ione, može biti gorivo u gorivnom članku.
Oksidansi[uredi | uredi kôd]
Oksidans u gorivnom članku može biti svaka kemijska tvar koja ima jaki afinitet za elektrone i koja redukcijom prelazi u ionsko stanje. Kisik je najčešći oksidans. Upotreba zraka kao oksidansa nameće dodatni problem odvođenja dušika koji ne sudjeluje u reakciji. U nekim se reakcijama kao oksidansi upotrebljavaju halogeni elementi (Cl, Br, F) ili oksidirani oblik nekog redoks - sustava, npr. Fe3+ u Fe3+/Fe2+, Ce4+ u Ce4+/Ce3+. Redoks sustavi obično se upotrebljavaju u sekundarnim gorivnim člancima, u kojima se produkti regeneriraju elektrolizom ili Sunčevom energijom na poluvodičkim elektrodama.
Stupanj djelovanja[uredi | uredi kôd]
Stupanj djelovanja (efikasnosti) gorivnog članka može se definirati na nekoliko načina, tj. kao termodinamički, naponski ili faradayski stupanj djelovanja.
Termodinamički stupanj djelovanja[uredi | uredi kôd]
Maksimalna moguća energija koja se može dobiti iz neke kemijske reakcije, tzv. slobodna energija kemijske reakcije, ΔG, definira se na sljedeći način: ΔG = ΔH - TΔS, gdje je ΔH ukupna oslobođena energija (reakcijska entalpija), T reakcijska temperatura (izoterma reakcija), a ΔS promjena entropije. Za elektrokemijske konvertere energije (baterije, gorivni članci) vrijedi ΔG = -nFE, gdje je n broj ekvivalenta (jednak broju elektrona) određen reakcijskom jednadžbom, F količina elektriciteta vezana uz jedan ekvivalent (Faradayeva konstanta), a E elektromotorna sila članka. Termodinamički stupanj djelovanja gorivnog članka (koji se još naziva i intrinzička djelotvornost) definira se izrazom: ήi = ΔG/ΔH. Gorivni članci imaju velik termodinamički stupanj djelovanja. Procesi u njima ne podliježu nekim ograničenjima, pa je djelotvornost konverzije energije znatno veća nego u direktnom izgaranju goriva gdje ta ograničenja postoje.
Naponski stupanj djelovanja[uredi | uredi kôd]
Zbog unutrašnjeg otpora (otpor elektrolita, otpor reakcijskog sloja elektroda, energije aktivacije ionskih reakcija itd.) pojavljuje se unutrašnji pad napona, pa je napon V na stezaljkama manji od elektromotorne sile E. Kada je reakcija u gorivnom članku beskonačno spora (kada struja teži 0), napon na stezaljkama jednak je elektromotornoj sili. Na temelju toga definira se naponski stupanj djelovanja gorivnog članka kao: ήV = V/E.
Faradayski stupanj djelovanja[uredi | uredi kôd]
Faradayski stupanj djelovanja gorivnog članka jest mjera za potpunost iskorištenja goriva u onoj elektrokemijskoj reakciji koja daje električnu struju. Definiran je kao: ήF= Q/Qm ; gdje je Q količina elektriciteta (C, As) dobivena iz gorivnog članka, a Qm količina elektriciteta koja bi se mogla dobiti iz goriva utrošenog samo u pretpostavljenoj elektrokemijskoj reakciji. Q je uvijek manje od Qm zbog toga što se najčešće ne postiže stahiometrijska potpunost elektrokemijske reakcije ili što se ponekad uz glavnu elektrokemijsku reakciju odvijaju i paralelne, elektrokemijski manje djelotvorne reakcije.
Ukupni stupanj djelovanja[uredi | uredi kôd]
Ukupni stupanj djelovanja gorivnog članka definiran je kao umnožak prethodnih triju stupnjeva djelotvornosti: ήT = ήi × ήV × ήF. Ukupni stupanj djelovanja niži je od termodinamičkog uglavnom zbog unutrašnjeg pada napona i nepoželjnih promjena koje nastaju u članku tijekom rada. Do sada postignuti ukupni stupanj djelovanja gorivnog članka tipa vodik – kisik jest oko 0,60.
Podjela gorivnih članaka[uredi | uredi kôd]
Prema načinu rada[uredi | uredi kôd]
Prema načinu rada gorivni se članci razvrstavaju na primarne i sekundarne. U primarnim gorivnim člancima gorivo i oksidans dovode se iz vanjskih spremnika, a produkt reakcije se odbacuje. U sekundarnim, regenerativnim gorivnim člancima produkt reakcije se regenerira u polazne reaktante uz utrošak energije (npr. termičke, električne).
Za regeneraciju se može upotrijebiti i Sunčeva energija, te radijacijska energija iz nuklearnih reaktora ili fisionih produkata dugog vremena poluraspada. Produkti se mogu regenerirati u gorivnom članku ili izvan njega, kontinuirano ili u ciklusima. Primarni gorivni članci slični su po principu rada bateriji, po tome što su oboje proizvođači električne energije. Sekundarni gorivni članci slični su akumulatoru jer su oboje samo sredstvo za posredno uskladištavanje energije.
Prema vrsti elektrolita[uredi | uredi kôd]
- Gorivni članci s alkalnim elektrolitom

- Gorivni članci s fosfornom kiselinom (PAFC)
- Gorivni članci s polimernom membranom kao elektrolitom (PEMFC)
- Gorivni članci s rastaljenim karbonatima kao elektrolitom (MCFC)
- Gorivni članci s čvrstim oksidima kao elektrolitom (SOFC)

Primjena gorivnih članaka[uredi | uredi kôd]
Gorivni članci intenzivno se ispituju, a istraživanja su dobila novi poticaj zbog zaoštravanja svjetske energetske krize. Međutim, za sada ne postoje tehnička rješenja gorivnih članaka, koja bi udovoljavala svim zahtjevima za visoku specifičnu snagu, pouzdanost i ekonomičnost i koji bi u tome mogli konkurirati procesima s neposrednim izgaranjem goriva (kotlovi s parnim turbinama, motori s unutarnjim izgaranjem, plinske turbine). Opravdanost upotrebe gorivnih članaka u budućnosti temelji se na dva čimbenika: visoki stupanj djelovanja i mali negativni utjecaj na okoliš. Stupanj djelovanja znatno je viši nego u svim do sada upotrebljavanim termičkim procesima za proizvodnju električne energije. Količina otpadne topline iz gorivnih članaka manja je nego iz konvencionalnih postrojenja, a produkti izgaranja ne sadrže štetne sastojke. Sastav produkata koji napuštaju gorivni članak, kada u gorivu ima ugljika, ovisi o postignutoj potpunosti izgaranja. Gorivni članci osim toga rade skoro bešumno. Prije široke primjene gorivnih članaka, osim niza manjih poteškoća, treba riješiti dva ključna problema. Prvi je zamjena plemenitih metala, platine i platini srodnih metala kao materijala elektroda, s drugim, jeftinijim i pristupačnijim materijalima. Drugi je problem trajnost i pouzdanost gorivnih članaka. Ova svojstva ovise o katalitičkoj aktivnosti elektrodne površine, o mogućnosti njenog obnavljanja nakon nepredviđenog, slučajnog onečišćivanja kemijskim spojevima, katalitičkim otrovima, iz goriva. Međutim, da održe radnu temperaturu, oni moraju ili neprekidno raditi, što snizuje njihov ukupni stupanj iskorištenja goriva, ili zahtijevaju pomoćne izvore energije. Ako se uspješno riješe spomenute teškoće, najvjerojatnije će se gorivni članci najprije upotrebljavati za pogon cestovnih vozila. Tada bi pogonski motor bio istosmjerni električni motor napajan iz gorivnog članka. Gorivo i oksidans preuzimali bi se u spremnike vozila u crpnimn stanicama koje bi odgovarale današnjim benzinskim postajama. Razmatra se mogućnost upotrebe gorivnih članaka s vodikom kao gorivom za stabilna postrojenja velike snage. Vodik bi se proizvodio elektrolizom vode upotrebljavajući neiskorištene snage termoelektrana, u prvom redu nuklearnih, u razdobljima malih opterećenja u elektroenergetskom sustavu.

Vodik bi trebao postati najčešći pogon, danas alternativni, a u budućnosti standardno pogonsko gorivo automobila. Brojni proizvođači automobila već uvelike obavljaju ispitivanja svojih automobila koje bi u bliskoj budućnosti mogao pokretati vodik. Najdalje u tome otišli su stručnjaci u Mazdi, Toyoti, BMW-u, Audiju, Fordu, General Motorsu, ali i mnogim drugim tvrtkama. Učinak većine takvih osobnih automobila još je ograničen i dosta će ovisiti o razvoju ove tehnologije i njenoj masovnoj upotrebi, a isto tako će i cijena odigrati važnu ulogu u kupnji automobila na vodik. Npr. Opel Hydra Gen 3 juri brzinom od 150 km/h i s jednim punjenjem spremnika ima doseg od 400 km. Autobusi s gorivnim člancima već su obavili praktična ispitivanja. Od 2002. u više europskih gradova u redovitom su prometu autobusi Citaro tvrtke Daimler-Chrysler kojima više nisu potrebne osovine, jer se svaki kotač pokreće vlastitim motorom. Oni imaju na krovu posude pod visokim tlakom u kojima je uskladišten vodik.

Veća je primjena moguća u obliku kombiniranih kogeneracijskih uređaja s prirodnim plinom za kućnu proizvodnju električne energije i topline koji bi u budućnosti opskrbljivali toplinom i električnom energijom jednu ili više obitelji. Tvrtka Valliant u laboratorijskim pokusima ispituje praktičnu upotrebljivost uređaja s gorivnim člancima za stambene zgrade. Švicarska tvrtka Sulzer Hexis otišla je korak dalje i njezin model HXS 1000 već se proizvodi u malim serijama. Uređaj je velik kao kotao za grijanje i prikladan je za svaku stambenu zgradu.
Minigorivni članak kao prijenosnu električnu centralu mnogi smatraju uspjehom tehnike, koji najviše obećava. Tako je kanadska tvrtka Ballard Power sa svojim Nexa Power Module (snaga 1,2 kw počela proizvoditi prvi izvor električne energije u većim količinama. Uređaj je velik kao štruca kruha, a gorivo je uskladišteno u sićušnim kutijicama i s njim, (neovisno o električnoj mreži, baterijama ili punjivim akumulatorima) mogu se neograničeno upotrebljavati prijenosna računala, televizori ili pokretni telefoni.

Vidi još[uredi | uredi kôd]
Vanjske poveznice[uredi | uredi kôd]
- BlueGEN Australska tvrtka koja proizvodi keramičke gorivne članke za široku uporabu Arhivirana inačica izvorne stranice od 28. srpnja 2011. (Wayback Machine)
- Baterije - tehnologija i održavanje Autor: Željko Harjač, Info-Mob.com

