Neutronski broj
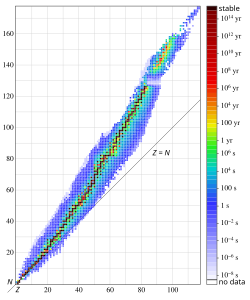

Neutronski broj ili broj neutrona (oznaka N) je broj neutrona u atomskoj jezgri. Atomi istoga kemijskog elementa s različitim brojem neutrona jesu izotopi, a atomi različitih kemijskih elemenata s jednakim brojem neutrona jesu izotoni.[1]
Atomska teorija[uredi | uredi kôd]
U atomskoj teoriji materije, atom se sastoji od atomske jezgre oko koje kruže elektroni. Danas je općenito priznato mišljenje da se atomska jezgra svih kemijskih elemenata sastoji od pozitivno nabijenih protona i neutrona koji nemaju električni naboj. Čestice koje se nalaze u atomskoj jezgri, to jest protoni i neutroni, zovu se zajedničkim imenom nukleoni (lat. nucleus: jezgra). Neutron ima masu gotovo jednaku masi protona. Proton je jezgra vodikovog atoma, pa mu je masa jednaka masi atoma vodika. Broj protona u atomskoj jezgri koji se zove atomski broj, jednak je njezinom električnom naboju i uvijek odgovara rednom broju kemijskog elementa u periodnom sustavu. Dakle atomskim brojem određena je vrsta kemijskog elementa.
U neutralnom atomu broj elektrona što kruže oko jezgre jednak je broju protona u jezgri. Pozitivan naboj jednog protona jednako je velik kao negativan naboj elektrona. 1869. ruski kemičar D. I. Mendeljejev otkrio je zakonitost ponavljanja kemijskih svojstva elemenata kod povećanja njihove atomske mase. On je tada sve poznate elemente poredao po rastućim atomskim masama jedan iznad drugoga i sastavio periodičku tablicu. Mendeljejev je dokazao da svaki kemijski element ima određen sastav atoma koji označuje atomska masa i mjesto u periodnom sustavu elemenata.
Broj protona P i neutrona N u jezgri određuje atomsku masu A određenog elementa, to jest:
i zove se maseni broj atoma. Na primjer jezgra helija sastoji se od dva protona i dva neutrona. Prema tome je električni naboj jezgre i redni broj helija 2, a relativna atomska masa 4. Oko atomske jezgre kruže negativno nabijeni elektroni, a broj elektrona jednak je broju protona u jezgri.
No kod istog broja protona u jezgri mogu postojati različite količine neutrona. Dva atoma koji imaju isti broj protona, a različiti broj neutrona, imaju skoro ista kemijska svojstva i isti redni broj, ali različite atomske mase. Takvi se elementi koji imaju isti redni broj, a različitu atomsku masu, zovu izotopi. Tako na primjer postoji klor koji ima redni broj 17, to jest njegova jezgra sadrži 17 protona, dok mu je atomska masa 35, što znači da jezgra njegova atoma sadrži 18 neutrona (17 + 18 = 35). Međutim, postoji i klor s atomskom masom 37, to jest jezgra njegova atoma sadrži 20 neutrona (17 + 20 = 37). Običan klor koji se nalazi u spojevima u prirodi ima atomsku masu 35,46, što znači da je on smjesa tih dvaju izotopa koji su u njemu zastupani u omjeru 3 : 1, to jest:
Prvi izotop klora pišemo simbolički 17Cl35, a drugi 17Cl37. Gornji broj uz kemijski simbol elementa znači relativnu atomsku masu tog elementa, a donji - broj protona u jezgri tog elementa, odnosno njegov redni broj. I vodik ima svoje izotope: 1H1 obični vodik, 1H2 teški vodik ili deuterij i 1H3 tricij.
Ovakvi izotopi nađeni su gotovo kod svih kemijskih elemenata. Tako uranij, koji je najvažniji u dobivanju nuklearne energije, ima 5 izotopa. Uranij ima redni broj 92, a njegovi izotopi imaju atomske mase 234, 235, 237, 238 i 239. U prirodnom uraniju najjače je zastupljen izotop s atomskom masom 238. Ima ga 137 puta više nego izotopa s atomskom masom 235. Ostalih njegovih izotopa ima još i manje. Izotopi se danas vrlo mnogo primjenjuju u medicini, tehnici i privredi, a naročito su veoma važni u proizvodnji nuklearne energije. Odjeljivanje izotopa vrši se centrifugiranjem, destilacijom, difuzijom i tako dalje.
Da se jezgra atoma koja se sastoji od pozitivno nabijenih protona ne razleti, jer se istoimeni električni naboji međusobno odbijaju, uzrok su privlačne sile koje vladaju, između protona i neutrona. To su takozvane sile jezgre ili osnovne sile koje, iako su vrlo velike, djeluju samo na vrlo male daljine, to jest u dimenzijama atomske jezgre. Tumačenje tih sila spada danas u glavne probleme atomske fizike.[2]


