Portal:Kemija/Prijašnji izdvojeni članci/2007.
Travanj

Rotacijska spektroskopija obuhvaća spektroskopske tehnike kojima se mogu proučavati rotacije molekula: mikrovalna spektroskopija i Ramanova spektroskopija.
Svaka molekula u plinskoj fazi može rotirati. U krutinama i tekućinama, molekulske rotacije su ili ometene ili zakočene interakcijama s drugim molekulama. Čak i slobodne molekule, se ne mogu rotirati na bilo koji način: molekulske vibracije su kvantizirane. Molekula može imati samo određene kutne količine gibanja. To znači da molekule imaju diskretne razine rotacijske energije. Apsorbiranjem ili emitiranjem kvanta energije u obliku fotona, molekula može prijeći iz jedne rotacijske energijske razine u drugu: molekula će ubrzati ili usporiti rotaciju za točno određenu vrijednost.
Elektromagnetsko zračenje, kao val električnog i magnetskog polja u prostoru, može intereagirati jedino s objektima s promjenjivim električnim ili magnetskim poljem. Da bi elektromagnetsko zračenje intereagiralo s molekulskim rotacijama, molekulske rotacije moraju proizvoditi promjenjivo električno polje u svojoj okolini (stalna magnetska polja kod molekula postoje samo kod iznimno rijetkih molekula), a to mogu samo molekule s trajnim električnim poljem. Najjače se sprežu molekule koje imaju trajni dipolni moment...Pročitaj cijeli članak | Prijašnji izdvojeni članci
Svibanj

Fazni dijagram je termin koji se rabi u fizikalnoj kemiji, mineralogiji i znanosti o materijalima, a označava tip grafa koji pokazuje ravnotežna stanja među termodinamički različitim fazama.
Najjednostavniji fazni dijagrami su dijagrami tlaka i temperature neke jednostavne tvari kao što je voda. Osi odgovaraju tlaku i temperaturi. Fazni dijagram pokazuje, u poljima tlaka i temperature, ravnotežne linije ili granice faza između tri faze: krute, tekuće i plinovite. Oznake na faznom dijagramu pokazuju točke gdje slobodna energija nije analitička. Otvoreni prostori, gdje je slobodna energija analitička funkcija, odgovaraju fazama. Faze su razdvojene linijama neanalitičnosti, gdje se pojavljuje fazni prijelaz, zbog čega se nazivaju granicama faza. Na dijagramu, granica između tekuće i plinovite faze ne nastavlja se u beskonačnost, nego se prekida u točki koja se naziva kritična točka. To odražava činjenicu da se na ekstremno visokim temperaturama i tlakovima tekuća i plinovita faza ne mogu razlikovati. Tu fazu nazivamo superkritični fluid. Za vodu kritična točka nalazi se na 647 K i oko 22,064 MPa. Postojanje kritične točke tekućine i plina otkriva neznatnu dvoznačnost u gornjoj definiciji. Kada se ide od tekuće prema plinovitoj fazi, obično se prjeđe fazna granica, ali moguće je odabrati put koji nikad ne prelazi granicu idući ravno..Pročitaj cijeli članak | Prijašnji izdvojeni članci
Lipanj

Osiromašeni uranij je uranij koji ima smanjen udio izotopa uran-235. Imena poput "Q-metal", "depletalloy" i "D-38", koja su se odnosila na osiromašeni uran, nisu više u uporabi.
Osiromašeni uranij je sporedni proizvod procesa obogaćivanja prirodnog urana za uporabu u nuklearnim reaktorima. Kada se ukloni većina fisibilnog radioaktivnog izotopa iz prirodnog urana, ostatak se zove osiromašeni uran. Manje uobičajen izvor tog materijala je prerađeno potrošeno nuklearno gorivo. Porijeklo osiromašenog urana može biti utvrđeno na temelju sadržaja uranija-236. Kao toksičan i radioaktivni otpadni proizvod koji zahtjeva dugotrajno skladištenje kao nuklearni otpad, osiromašeni uran je skup za skladištenje, ali ga je relativno jeftino proizvesti. Uopćeno gledajući jedini pravi troškovi su oni koji su vezani za dobijanje metalnog urana iz UF6. Njegova izuzetno velika gustoća, malo manja od gustoće volframa, i njegova niska cijena čine ga primamljivim za mnoštvo upotreba. Međutim, materijal je sklon koroziji i njegove male čestice su zapaljive...Pročitaj cijeli članak | Prijašnji izdvojeni članci
Srpanj

Opća formula karboksilnih kiselina je R-COOH. Pri čemu je R- ugljikovodični lanac, i -COOH karboksilna skupina karakteristična za sve karboksilne kiseline.
Karboksilne kiseline mogu biti mono-, di- i poli-karboksilne kiseline ovisno o broju -COOH skupina a dijele se na zasićene, nezasićene i aromatske. No karboksilne kiseline su općenito slabe kiseline iako imaju oštar i neugodan miris.
Karboksilne kiseline imenuju se tako da se ispred nastavka -ska kiselina doda ime alkana ovisno o broju ugljikovih atoma. Tako će na primjer kiselina s 3 C atoma po alkanu propanu biti imenovana propanska kiselina iako je njeno puno češće korišteno ime propionska ili mliječna kiselina (jer ju nalazimo u mlijeku).
Karboksilnih kiselina ima mnogo...Pročitaj cijeli članak | Prijašnji izdvojeni članci
Kolovoz

Elektronski omotač atoma je slojeviti omotač oko jezgre atoma u kojemu se nalaze elektroni. Broj elektrona u omotaču ovisi o elementu atoma (npr. vodik ima jedan proton pa tako i jedan elektron).
Elektroni zbog svojeg negativnog naboja kruže oko jezgre atoma ali radi povoljnijeg energetskog rasporeda kruže u slojevima ili ljuskama. Za sada postoji 7 energetskih ljusaka u koje se elektroni mogu rasporediti: K, L, M, N, O, P, Q. Ljuska K ima samo 2 elektrona a dalje idu po formuli 2n2 (gdje je n broj ljuske). Tako L ljuska ima 8 e-, M ljuska 18 e-, N ljuska 32 e-, O ljuska 50 e-, P ljuska 72 e- a (posljednja) energetska ljuska Q može primiti čak 98 e-...Pročitaj cijeli članak | Prijašnji izdvojeni članci
Rujan
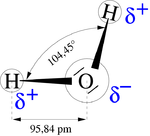
Voda je kemijski spoj dva atoma vodika i jednog atoma kisika. Kemijska formula vode je H2O.
Ima talište na 0ºC (273K) i vrelište na 100ºC (373K).
Na Zemlji tvori oceane, rijeke, oblake i polarne kape. Voda pokriva 71% zemljine površine i nužna je za život kakav poznamo. Ona je po težini najobilnija sastavnica stanica i organizama (75-85%), a veliki broj stanica ovisi o izvanstaničnoj okolini koja je također uglavnom vodena. Najveća gustoća vode je pri 4°C.
Otapalo je tekućina u kojoj se druga otopljena tvar može otopiti. Voda zbog polarnosti posjeduje izvrstan kapacitet da otapa različite vrste tvari.
- * Hidrofilne otopljene tvari su one koje voda privlači, pa se uslijed hidratacije brže otapaju u vodi (male organske molekule u stanicama: šećeri, organske kiseline i neke aminokiseline). To su polarnostpolarne, ili specifične neutralne molekule, koje elektrostatički međudjeluju s molekulama vode.
Listopad

Otopine su homogene smjese dvaju ili više sastojaka pri čemu je jedan sastojak u velikom suvišku (otapalo). Tvari koje nisu u suvišku su otopljene tvari ili soluti. Molekule soluta su međusobno izolirane zbog velike većine molekula otapala, tako da otapalo diktira svojstva otopljenih tvari u otopini.
Uobičajeni primjeri su kuhinjska sol ili šećer koji su krutine otopljeni u vodi koja je tekućina. U tekućinama se također mogu otapati i plinovi, npr. ugljikov dioksid i kisik u vodi, dok se između sebe plinovi otapaju bez ograničenja. Primjeri krutih otopina su mnoge slitine i minerali. Sposobnost otapanja tvari u nekom otapalu naziva se topljivost.
Pojam otopina se u nekim područjima kemije upotrebljava..Pročitaj cijeli članak | Prijašnji izdvojeni članci
Studeni

Goriva su sve tvari koje sagorijevanjem daju toplinu. Toplinska energija dobiva se iz goriva kemijskim procesom koji se zove oksidacija ili gorenje. U najviše slučajeva oksidacija je spajanje gorive tvari i kisika. Gorive tvari su najvećim dijelom ugljici pa je gorenje spajanje kisika (gorive tvari) s ugljikom. I ne-ugljična goriva kao vodik, klor, amonijak, natrij..., spajanjem s kisikom oksidiraju i oslobađaju toplinu. Prilikom oksidacije dolazi do kemijske reakcije, promjene u strukturi atoma goriva i oksidatora (kisika) te se takva goriva svrstavaju u kemijska goriva.
Isprva se energija dobivala od vjetra, vode, vodene pare ili sunca. Najčešći izvor za dobivanje energije bili su drva i ugljen koji su se koristili za pogon brodova, lokomotiva i termoelektrana. 1823. godine braća Budinin destilacijom nafte dobivaju ulje za rasvjetu, petrolej. Prvu petrolejsku svjetiljku konstruirao je 1848. Poljak Ignacy Łukasiewicz a prvu bušotinu nafte izgradio je Edwin L. Drake 27. kolovoza 1859. u Titusville-u (SAD). Poslije pronalaska Otto-motora dolazi do naglog povećanja potrošnje naftnih derivata.
Prosinac

Vibracijska spektroskopija je grana spektroskopije koja proučava spektre, koji su uzrokovani vibracijama molekula. To obuhvaća infracrvenu spektroskopiju i Ramanovu spektroskopiju.
Sve molekule vibriraju. Molekulske vibracije, za razliku od vibracija makroskopskih tijela, su kvantizirane. Molekula može vibrirati točno određenim amplitudama, koje odgovaraju vibracijskim energijskim razinama. Spektroskopski prijelaz se može dogoditi jedino ako je energija apsorbiranog ili emitiranog fotona jednaka razlici dviju vibracijskih energijskih razina (Bohrov uvjet), odnosno ako je razlika energija raspršenog i dolazećeg fotona jednaka razlici energijskih razina.
Ukoliko vibracija molekule uzrokuje promjenu dipolnog momenta molekule, vibracija će se sprezati s elektromagnetskim zračenjem i doći će do apsorpcije ili emisije zračenja. Takva vibracija će biti aktivna u infracrvenom spektru. Vibracija će biti aktivna u Ramanovom spektru ako vibracija uzrokuje promjenu polarizabilnosti molekule. Elektromagnetsko zračenje se može sprezati i s kvadrupolnim ili magnetskim momentom, ali ta sprega je vrlo slaba, pa je takve vibracije izuzetno teško proučavati.
