Benzen: razlika između inačica
m robot Mijenja: sl:Benzen |
m robot Mijenja: ml:ബെൻസീൻ |
||
| Redak 74: | Redak 74: | ||
[[lv:Benzols]] |
[[lv:Benzols]] |
||
[[mk:Бензен]] |
[[mk:Бензен]] |
||
[[ml:ബെൻസീൻ]] |
|||
[[ml:ബെന്സീന്]] |
|||
[[ms:Benzena]] |
[[ms:Benzena]] |
||
[[nl:Benzeen]] |
[[nl:Benzeen]] |
||
Inačica od 7. veljače 2010. u 00:02
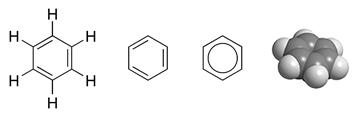
Benzen je najjednostavniji aromatski ugljikovodik. Empirijska formula mu je C6H6.
Znanstvenici su dugo pokušavali odrediti strukturnu formulu. Njemački kemičar Friedrich August Kekulé von Stradonitz to je postigao tako da je naizmjenice postavio jednostruke i dvostruke veze između atoma ugljika.
Može se crtati i s jednostrukom vezom između atoma ugljika i kružnicom unutar šesterokuta što se naziva benzenov prsten. Svi aromatski ugljikovodici imaju jedan ili više benzenovih prstenova.
Dobivanje
- Frakcijskom destilacijom katrana kamenog ugljena
- Sintezom tri molekule etina (C2H2)
Svojstva
Benzen je bezbojna tekućina, jakog mirisa. Vrije na 80 °C. Skrućuje se u bijelu kristalnu tvar. U vodi se ne otapa ali se otapa u organskim otapalima.
Benzen otapa masti i ulja, smole i boje.
Benzenove pare su veoma otrovne i uzrokuju leukemiju. Proizvodi dobiveni iz benzena nisu otrovni kao benzen.
Lako je zapaljiv. Zapaljen gori čađavim plamenom.
- 2C6H6 + 15O2 → 12CO2 + 6H2O
Zbog postojanja jednostrukih i dvostrukih veza stupa u reakcije adicije i supstitucije.
Supstitucija:
- C6H6 + Br2 → C6H5Br + HBr
Adicija:
- C6H6 + 3Cl2 → C6H6Cl6
Upotreba
Koristi se kao otapalo, zatim za proizvodnju lijekova, boja, lakova, plastičnih masa, eksploziva, sredstava za pranje , insekticida
