Drugi zakon termodinamike



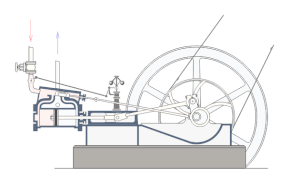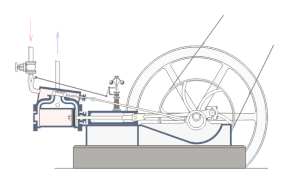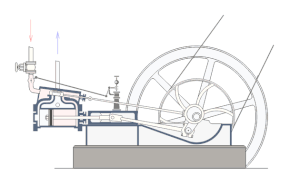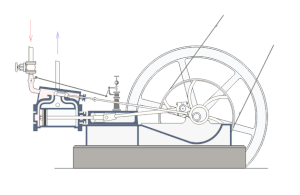
Drugi zakon termodinamike upućuje na smjer u kojem se odvija pretvorba toplinske energije u mehaničku. Do toga je zakona došao već Carnot 1824. On je proučavao idealne uvjete prelaska topline u mehanički rad i zaključio da su za prelazak topline u rad potrebna dva spremnika topline na različitoj temperaturi; prelaskom topline iz toplijega spremnika u hladniji samo se dio topline pretvara u rad, a ostatak topline prelazi u spremnik niže temperature (degradacija). Prema Carnotu, maksimalna djelotvornost η idealnoga toplinskoga stroja, koji kružnim procesom pretvara toplinu u rad, iznosi:
gdje su: T1 i T2 temperature toplijega i hladnijega spremnika; Q1 je toplina koja pri prelasku stoji na raspolaganju, a Q2 dio topline koji se degradira. Bit je drugoga zakona termodinamike da se pri prelasku topline u rad dio topline uvijek gubi ili degradira (degradacija). Matematički izraz drugoga zakona termodinamike iskazuje se s pomoću entropije. Za sustav temperature T, u kojem se nalazi ukupna količina topline Q, entropija S izražava se kao:
Iz toga slijedi da je entropija sustava to veća što mu je, uz danu količinu topline u sustavu, temperatura niža. Kako pri svakom prelasku topline u rad dio topline prelazi u spremnik niže temperature, ukupna se entropija sustava povećava. Poopćenjem drugoga zakona može se reći da se entropija zatvorenoga sustava povećava pri svakom procesu.[1]
Drugi zakon termodinamike se može pojednostavljeno objasniti:
Osim gornjeg, Rudolf Clausius dao je još nekoliko objašnjenja ovog zakona:
S protokom vremena, ukupna entropija termički zatvorenog sustava koji nije u termodinamičkoj ravnoteži uvijek raste, težeći da dosegne najveću moguću vrijednost. Vjerojatno najpopularnija formulacija ovog zakona glasi:
Formulacija Lorda Kelvina:
Ova formulacija drugog zakona termodinamike često se izražava kao:
Perpetuum mobile druge vrste bio bi upravo takav uređaj koji bi samo uzimao toplinu iz spremnika topline i pretvarao tu toplinu u rad.
Objašnjenje[uredi | uredi kôd]
Prvi zakon termodinamike kaže da se mehanički rad može pretvoriti u toplinu, odnosno toplina u mehanički rad, i da između topline i mehaničkog rada postoji određeni odnos. Ali ovaj stavak ne govori ništa o tome pod kojim se uvjetima pretvara toplina u rad i obratno. Uvjete i mogućnost tog pretvaranja određuje drugi glavni stavak termodinamike. Iz Carnotovog kružnog procesa vidjeli smo da se sva toplina ne može pretvoriti u mehanički rad, i da je za mehanički rad potreban pad temperature. Da bi se iz topline dobio mehanički rad, potrebna su dva spremnika, jedan s višom, a jedan s nižom temperaturom, jer toplina uvijek prelazi s tijela više na tijelo niže temperature. Toplina koja odlazi u spremnik niže temperature gubi sposobnost pretvaranja u mehanički rad, pa kažemo da je ona degradirana. To znači da proces pretvaranja topline u mehanički rad nije reverzibilan (obratljiv) nego ireverzibilan (neobratljiv). Reverzibilni su oni toplinski procesi gdje se plin vraća u svoje prvobitno stanje bez ikakvih gubitaka. Obrnuto su ireverzibilni procesi. Taj se proces vrši pomoću toplinskih strojeva koji vrše radnju periodički, ali uvijek tako da se čitava toplina ne pretvara u rad već jedan dio ostaje neiskorišten. Uzrok tome nije nesavršenost toplinskih strojeva već je to posljedica prirodnog zakona, to jest drugog glavnog stavka termodinamike koji glasi:
Drugi zakon termodinamike isključuje takozvani perpetuum mobile druge vrste. Nije, naime, moguće sagraditi stroj koji bi stvarao rad na račun topline okoline bez razlike temperature, to jest bez spremnika niže temperature. Kad bi se to moglo, brod bi mogao ploviti na račun golemih količina topline sadržanih u moru i to bez ikakvog goriva.
U prirodi se stalno zbivaju toplinski procesi kod kojih toplina prelazi s toplijih tijela na hladnija. Na taj se način temperature sve više izjednačuju, i vrši se stalna degradacija topline jer ne postoji mogućnost za njeno pretvaranje u mehanički rad. Ovakva stalna degradacija topline mogla bi konačno dovesti do potpunog izjednačenja sviju temperatura i tako do općeg mrtvila u prirodi koje se zove toplinska smrt. Tako su ljudi zaključivali dok još nisu poznavali nuklearnu ili atomsku energiju. U prirodi postoje i nuklearni procesi koji se na primjer zbivaju na zvijezdama i na Suncu, kod kojih se ponovo stvaraju visoke temperature. Izjednačenje svih temperatura moglo bi jedino nastati samo u malim pojedinim dijelovima svemira, i to ne bi bilo trajno.[2]


