Otopine

Otopina u širem smislu je homogena smjesa u kojoj se sastojci nalaze u molekularnom (prava otopina) ili koloidnom razdjeljenju (koloidna otopina) i koja može biti u sva tri agregatna stanja: plinska smjesa, smjesa kapljevina, čvrsta otopina (npr. srebra u zlatu, vodika u metalu paladiju).
Otopina u užem smislu je samo tekuća otopina, ponajprije ona nastala otapanjem čvrste tvari u otapalu.[1]
Otapalo i otopljena tvar[uredi | uredi kôd]
Osnovno je svojstvo svih pravih otopina homogen sastav, što znači da npr. otopina etanola u vodi u svakom svom djeliću ima jednak sastav, odnosno da je svuda u otopini omjer broja molekula etanola i vode stalan. U otopinama valja razlikovati otapalo i otopljenu tvar. Ako su otapalo i otopljena tvar tekućine, otapalom se najčešće naziva onaj sastojak kojeg u otopini ima više. Inače, pod otapalom se razumije tekućina, a pod otopljenom tvari kruta ili plinovita tvar koja se u toj tekućini otapa.
Vrste otopina[1][uredi | uredi kôd]

Tekuće tvari (kapljevine) se mogu među sobom otapati (miješati) potpuno (u svim omjerima) ili u ograničenoj mjeri. Topljivost kapljevina koje se ne miješaju u svim omjerima redovito se mijenja s temperaturom, te na određenoj temperaturi može postati potpuna (kritična točka topljivosti).
Čvrste se tvari redovito otapaju u otapalima u ograničenoj mjeri. Najveća količina čvrste tvari koja se pod danim uvjetima (ponajprije pri određenoj temperaturi) može otopiti u određenoj količini otapala naziva se topljivost te tvari pod tim uvjetima.
Otopina koja sadrži maksimalnu količinu otopljene tvari zove se zasićena, ona koja sadrži nešto manje, ali još uvijek velike količine otopljene tvari zove se koncentrirana, a ona koja sadrži male količine otopljene tvari zove se razrijeđena otopina. Koncentrirana i razrijeđena otopina spadaju u nezasićene otopine. U nekim je uvjetima moguće da otopina sadrži više otopljene tvari nego što bi odgovaralo topljivosti tada govorimo o prezasićenoj otopini. Otopine dakle mogu biti:
- zasićene
- nezasićene, koncentrirana i razrijeđena otopina
- prezasićene
Otopina plina u kapljevini načelno se ne razlikuje od smjese kapljevina; zakon linearne ovisnosti napona pare razrijeđene otopine o koncentraciji naziva se u tom slučaju Henryjevim zakonom.
Vrste otopina prema veličini čestica[uredi | uredi kôd]

Sve otopine u kojima je otapalo tekućina (voda) možemo podijeliti u tri disperzna sustava prema otopljenim ili raspršenim česticama:[2]
| Naziv sustava | Veličina čestica | Primjer |
|---|---|---|
| Suspenzija | > 200 nm | mutna riječna voda |
| Koloidna otopina | 1 - 200 nm | mlijeko, citoplazma |
| Prava otopina | <1 nm | morska voda, vino |
Topljivost tvari u otapalima[uredi | uredi kôd]
Voda je uobičajeno ali istovremeno vrlo osobito otapalo. Molekule vode su dipoli među kojima djeluje vodikova veza te je voda najpolarnije otapalo. Neka druga otapala su također polarna (alkoholi), slabo polarna (eteri) ili nepolarna (ugljikovodici). U vodi se zato dobro otapaju polarne odnosno ionske tvari, građene od nabijenih čestica iona a to su razne soli, kiseline, hidroksidi, dok se nepolarne tvari (jod, sumpor) ne otapaju ili ne miješaju (ugljikovodici, ulja). Obrnuto u nepolarnim ili slabo polarnim otapalima (ugljikovodici, eteri) slabo se otapaju ionske tvari a dobro se otapaju nepolarne kovalentne tvari (ulja, masti). Zato je postavljeno "zlatno pravilo" otapanja:
"Slično se otapa u sličnom!"[2]
Također vrijedi opčenito: topljivost krutih tvari raste porastom temperature otapala dok topljivost plinova pada.
Topljivost tvari u vodi[uredi | uredi kôd]
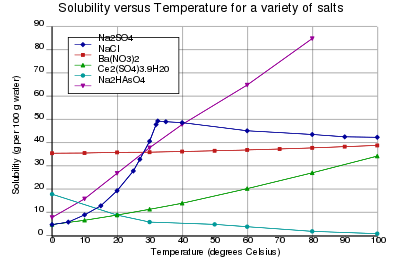
Topljivost tvari u vodi je znakovito svojstvo te tvari, izražava se u gramima otopljene tvari na 100 g vode pri promatranoj temperaturi. Topljivost može za različite tvari biti vrlo različita (netopljive, slabo topljive, jako topljive tvari), a redovito se mijenja s temperaturom: s porastom temperature najčešće se povećava, ali se može i smanjivati ili se u jednom temperaturnom intervalu povećavati, a u drugome smanjivati (dijagram).
Svojstva otopina[uredi | uredi kôd]
Svojstva otopine (npr. gustoća, vrelište) linearno se mijenjaju s njezinim sastavom samo onda kada su sastojci među sobom kemijski srodni, npr. u smjesama ugljikovodika (idealne otopine). U protivnom, postoje redovito znatna odstupanja od linearnosti (npr. neke smjese kapljevina vriju na temperaturi nižoj ili višoj od vrelišta bilo kojeg od njihovih sastojaka). Tada linearna ovisnost o sastavu postoji samo za razrijeđenu otopinu. S povećanjem koncentracije otopljene tvari smanjuje se tlak parâ otapala, što kao posljedicu ima sniženje temperature očvršćivanja i povišenje temperature vrelišta otopina. Ova dva svojstva otopina zajedno s osmozom ubrajamo u koligativna svojstva otopina. To su svojstva koja ovise jedino o broju otopljenih čestica a ne i o njihovoj kemijskoj ili fizikalnoj prirodi. [1]
Iskazivanje sastava otopina[uredi | uredi kôd]
Sastav otopina može se izraziti na razne načine:
- omjerima,
- udjelima,
- koncentracijama i
- molalnošću.
