Vinska kiselina

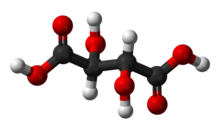
Vinska kiselina (HOOCCHOHCHOHCOOH, C4H6O6, E334) je bijela, kristalna organska dihidroksijantarna kiselina i jedna od najraširenijih biljnih kiselina. Prirodno se javlja u mnogim biljkama, a njezina kalijeva sol nalazi se u soku grožđa i glavni je sastav vinskog kamena.
Sirovi produkt naziva se birsa. Čisti produkt poznat je pod nazivom čista birsa.
Primjena[uredi | uredi kôd]
Koristi se u proizvodnji žbuke, gipsanih ploča i fasadnih smjesa gdje regulira brzinu sušenja.
Prirodno je biljno sredstvo za reguliranje kiselosti, sekvestrant i antioksidans. Dobiva se iz voća u kojem se nalazi kao slobodna kiselina ili vezana na kalij, kalcij ili magnezij. Uglavnom se dobiva kao nusprodukt u proizvodnji vina. Osamdeset posto ingestirane vinske kiseline unište crijevne bakterije, a preostala količina koja se apsorbira u krv izluči se urinom. Dopuštena je upotreba u ekološkoj proizvodnji namirnica. Namirnicama se dodaje uglavnom po pravilu quantum satis. Smatra se bezopasnom.
Dodaje se u hranu radi postizanja kiselog okusa, a koristi se i kao antioksidans.
Upotrebljava se prehrambenoj industriji (najviše u pekarstvu) - kao kisela komponenta za neke praške za pecivo (praške za pečenje), a sa sodom bikarbonom razvija ugljikov dioksid koji poboljšava tijesto.
Također se koristi i kod proizvodnje pjenušaca i vina, gdje ima važnu ulogu u spuštanju pH vrijednosti prilikom fermentacije što sprječava razvoj mnogih nepoželjnih bakterija, a nakon fermentacije djeluje kao konzervans.
Ovisno o vrti grožđa i mjestu gdje se sadi, nisu iste kiselosti mošta, pa se dodaje za povećanje kiselina u moštu i vinu, ali samo u određenim situacijama.
U vinarstvu se ubraja u nehlapljive kiseline. Poželjna u vinu, do određene granice. Ako je tih kiselina manje, što se događa u južnim hrvatskim krajevima, onda je dopustivo dokiseliti vino i obično se dodaje vinska kiselina.[1]
Priređivanje[uredi | uredi kôd]
Vinsku kiselinu prvi puta je iz kalijevog tartarata izolirao perzijski alkemičar Jabir Ibn Hayyan koji je također zaslužan i za brojne druge osnovne kemijske procese koji se i danas koriste. Birsa je bila poznata u stara vremena, no vinsku kiselinu prvi puta je izolirao modernim procesom 1769. švedski kemičar Carl Wilhelm Scheele.
Neutralizacijom natrijevim hidroksidom nastaje natrij-kalijev tartarat, poznat kao Seignetteova sol (Rochelle-sol, prema mjestu Rochelle u Francuskoj), a upotrebljava se kao purgativ.
Mezo- ili racemična vinska kiselina može se sintetski prirediti hidroksiliranjem maleinske ili furmarne kiseline s vodikovim superoksidom u prisutnosti volframovog oksida. Zagrijavanjem s alkalijama obje se forme mogu prevesti u ravnotežnu smjesu.
Fehlingova otopina pripravlja se iz bakrenog sulfata, natrijeva hidroksida i natrij-kalijeva tartara. Tartarat-ion stvara helatni kompleks koji smanjuje koncentraciju bakrenog iona ispod one potrebne za taloženje bakrenog hidroksida. Kompleksna sol nastaje nizom reakcija koje su analogne onima prilikom stvaranja bakrenog kompleksa s biuretom.
Poznat je i tzv. "vinski kamen" (kalijev kiseli tartarat KHC4H4O6) dobiven od vinske kiseline.
Izvori[uredi | uredi kôd]
- ↑ Prvi hrvatski vinogradarski portal Nenad Bižić: Pretok i bistrenje vina (pristupljeno 1. studenoga 2015.)
- Carl R. Noller; Kemija organskih spojeva. Glavni urednik: Zvonko Vistrička. Izdavač: Tehnička knjiga, listopad 1968.g. Zagreb. Str. 809.
