Masno tkivo

Masno tkivo ili adipozno tkivo jest vezivno tkivo sastavljeno većinom od adipocita.[1][2] Masne naslage u tijelu ljudi i životinja ponekad se nazivaju salo.[3] Osim adipocita, masno tkivo sadrži stromalne vaskularne frakcije (SVF) stanica, uključujući preadipocite, fibroblaste, vaskularne endotelne stanice i niz imunosnih stanica kao što su makrofagi masnoga tkiva. Masno tkivo nastaje iz preadipocita. Njegova je glavna uloga skladištenje energije u obliku lipida, iako također mehanički štiti i toplinski izolira tijelo. Budući da nije hormonski inertno, masno je tkivo posljednjih godina prepoznato kao glavni endokrini organ[4] jer proizvodi hormone kao što su leptin, estrogen, rezistin i citokine (osobito TNFα).[2] Kod pretilosti, masno tkivo uključeno je u kronično otpuštanje proupalnih markera poznatih kao adipocitokini, koji su odgovorni za razvoj metaboličkog sindroma i niza bolesti uključujući dijabetes tipa 2, kardiovaskularne bolesti i aterosklerozu.[2][5] Dvije vrste masnoga tkiva jesu bijelo masno tkivo (WAT), koje skladišti energiju, i smeđe masno tkivo (BAT), koje stvara tjelesnu toplinu. Čini se da je stvaranje masnog tkiva dijelom upravljano genom za masno tkivo WDTC1. Masno tkivo, točnije smeđe masno tkivo, prvi je opisao švicarski prirodoslovac Conrad Gessner 1551. godine.[6]
Anatomske značajke[uredi | uredi kôd]

U ljudi se masno tkivo nalazi ispod kože (potkožno masno tkivo), oko unutarnjih organa (visceralno masno tkivo), u koštanoj srži, unutar mišića i u dojkama. Osim adipocita, koji čine najveći udjel stanica unutar masnog tkiva, prisutni su i drugi tipovi stanica, zajednički nazvani stromalna vaskularna frakcija (SVF). Ona uključuje preadipocite, fibroblaste, makrofage masnog tkiva i endotelne stanice.
Masno tkivo sadrži mnogo malih krvnih žila. U pokrovnom sustavu, koji uključuje kožu, nakuplja se u najdubljem sloju, osiguravajući izolaciju od topline i hladnoće. Oko organa pruža zaštitu od potresanja. Ipak, njegova je glavna uloga skladištenje lipida, koji se mogu oksidirati kako bi zadovoljili energijske potrebe tijela i zaštitili ga od viška glukoze pohranjivanjem triglicerida koje proizvodi jetra od šećera; neki dokazi sugeriraju da je većina sinteze lipida iz ugljikohidrata nastaje u samome masnom tkivu.[7] Nakupine masnoga tkiva u različitim dijelovima tijela imaju različite biokemijske profile. U normalnim uvjetima ono mozgu šalje povratne informacije o gladi i uhranjenosti.
Masno tkivo ima gustoću ~0,9 g/ml. Dakle, osoba s više masnog tkiva lakše će plutati u vodi od osobe iste mase s više mišićnog tkiva koje ima gustoću 1,06 g/ml.[8]

Pretilost[uredi | uredi kôd]
U pretile osobe višak masnog tkiva koji visi s trbuha naziva se panikulus. Panikulus komplicira medicinske operacije nad morbidno pretilim osobama. Može ostati kao kožna pregača ako vrlo pretila osoba izgubi velike količine masnoga tkiva, što je česta posljedica operacije želučane premosnice. Pretilost se liječi vježbanjem, dijetom i bihevioralnom terapijom. Rekonstruktivna kirurgija jedan je način liječenja.[9]
Visceralno masno tkivo[uredi | uredi kôd]

Visceralno, intraabdominalno ili trbušno masno tkivo nalazi se unutar trbušne šupljine, nagomilano između organa (želudac, jetra, crijeva, bubrezi…). Visceralno masno tkivo razlikuje se od potkožnoga masnog tkiva i intramuskularnog masnog tkiva koje se nalazi u skeletnim mišićima. Masno tkivo u donjem dijelu tijela, u bedrima i stražnjici, potkožno je, dok je masno tkivo u abdomenu uglavnom visceralno i polutekuće.[10] Visceralno masno tkivo sastoji se od nekoliko masnih naslaga, uključujući mezenterijsko, pasjemenično bijelo masno tkivo (EWAT) i perirenalne nakupine. Visceralno masno tkivo često se mjeri svojom površinom u cm2 (VFA, za engleski visceral fat area).[11]
Višak visceralne masnoće poznat je kao abdominalna pretilost, a kod nje trbuh pretjerano strši. Nova mjerila kao što je body volume index (BVI) posebno su osmišljena za mjerenje volumena trbuha i abdominalnog masnog tkiva. Višak visceralne masnoće također je povezan s dijabetesom tipa 2,[12] inzulinskom rezistencijom,[13] upalnim bolestima,[14] i drugima.[15] Isto tako, pokazalo se da je nakupljanje masnog tkiva na vratu (ili cervikalnog masnog tkiva) povezano sa smrtnošću.[16] Nekoliko je studija sugeriralo da se visceralna masnoća može predvidjeti iz jednostavnih antropometrijskih mjera[17] i predviđa smrtnost točnije od indeksa tjelesne mase ili opsega struka.[18]
Muškarci imaju veću vjerojatnost da će imati masnoću pohranjenu na trbuhu zbog razlika u spolnim hormonima. Estrogen, ženski spolni hormon, kod žena uzrokuje pohranjivanje masti na stražnjici, bedrima i bokovima.[19][20] Kada žene dođu u menopauzu i opadne im estrogen koji proizvode jajnici, salo migrira sa stražnjice, bokova i bedara u struk;[21] kasnije se masnoća skladišti na trbuhu.[10]
Visceralna mast može biti uzrokovana viškom razine kortizola.[22] Najmanje 10 sati tjedno aerobne vježbe dovodi do smanjenja visceralne masnoće kod onih bez metaboličkih poremećaja.[23] Trening otpora i kalorijska restrikcija također smanjuju visceralnu masnoću, iako njihov učinak ne mora biti kumulativan.[24] I tjelovježba i hipokalorična dijeta uzrokuju gubitak visceralne masnoće, ali tjelovježba ima veći učinak na visceralnu masnoću u odnosu na ukupnu masnoću.[25] Vježbanje visokog intenziteta jedan je od načina za učinkovito smanjenje ukupne abdominalne masnoće.[26][27] Energetski ograničena dijeta u kombinaciji s tjelovježbom smanjit će ukupnu tjelesnu masnoću i omjer visceralnog masnog tkiva u odnosu na potkožno masno tkivo, što ukazuje na preferencijalnu mobilizaciju visceralne u odnosu na potkožnu masnoću.[28]
Epikardijalna mast[uredi | uredi kôd]
Epikardijalno masno tkivo (EAT) poseban je oblik visceralnog masnog tkiva taloženog oko srca. Utvrđeno je da je ono metabolički aktivan organ koji stvara različite bioaktivne molekule, koje mogu značajno utjecati na rad srca.[29] Uočene su značajne razlike ovoga tkiva u odnosu na potkožno masno tkivo, što ukazuje na utjecaj pohranjenih masnih kiselina specifičan za lokaciju na funkciju i metabolizam adipocita.[30]
Potkožno masno tkivo[uredi | uredi kôd]
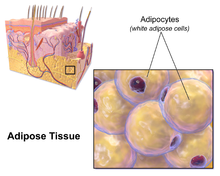
Većina preostale nevisceralne masti nalazi se ispod kože u području koje se naziva hipodermis.[31] Potkožno masno tkivo nije povezano s mnogim klasičnim patologijama povezanima s pretilošću, kao što su bolesti srca, rak i moždani udar, a neki dokazi čak sugeriraju da bi moglo biti zaštitno.[32] Uobičajeno ženski obrazac raspodjele tjelesne masnoće oko bokova, bedara i stražnjice potkožno je masno tkivo koje predstavlja manji zdravstveni rizik u usporedbi s visceralnom masnoćom.[33][34]
Kao i svi drugi organi masnoga tkiva, potkožno masno tkivo aktivan je dio endokrinog sustava koji luči hormone leptin i rezistin.[31]
Koštana srž[uredi | uredi kôd]
Masno tkivo koštane srži slabo je istraženo tkivo koje se nalazi u kosti i prošarano je krvotvornim (hematopoetskim) stanicama kao i koštanim elementima. Adipociti u ovoj nakupini potječu iz mezenhimalnih matičnih stanica (MSC) koje mogu postati stanice masnoga tkiva, stanice kosti kao i druge vrste stanica. Činjenica da se ovo tkivo povećava u uvjetima restrikcije kalorija/anoreksije značajka je koja ga razlikuje odtalih spremnika masnoćai.[35][36][37] Vježbanje regulira masno tkivo u koštanoj srži, smanjujući mu količinu i smanjujući veličinu adipocita koštane srži.[38][39][40] Regulacija masnoća koštane srži tjelovježbom sugerira da ona ima fiziološke sličnosti s drugim bijelim masnim naslagama. Njegovo povećanje kod pretilosti dodatno ukazuje na sličnost s naslagama bijeloga masnog tkiva.[38]
Ektopična mast[uredi | uredi kôd]
Ektopična mast je nakupina triglicerida u tkivima koja nisu masno tkivo, a koja bi trebala sadržavati samo male količine masnoća, kao što su jetra, skeletni mišići, srce i gušterača.[1] Ona može ometati stanične funkcije, a time i funkciju organa, a povezana je s inzulinskom rezistencijom kod dijabetesa tipa 2.[41] Pohranjuje se u relativno velikim količinama oko organa trbušne šupljine, ali ne smije se zamijeniti s visceralnim masnim tkivom.
Specifičan uzrok nakupljanja ektopične masnoće nije poznat. Uzrok je vjerojatno kombinacija genskih, okolišnih i bihevioralnih čimbenika koji su uključeni u prekomjeran unos energije i smanjenu tjelesnu aktivnost. Znatan gubitak mase može smanjiti ektopične zalihe masti u svim organima, a to je povezano s poboljšanjem funkcije tih organa.[41]
Neinvazivne metode mršavljenja poput dijete i tjelovježbe mogu smanjiti ektopičnu masnoću (osobito u srcu i jetri) kod djece i odraslih.[42][43]
Fiziologija[uredi | uredi kôd]
Slobodne masne kiseline oslobađaju se iz lipoproteina pomoću lipoproteinske lipaze (LPL) i ulaze u adipocit, gdje se ponovo sastavljaju u trigliceride, esterificirajući ih u glicerol.[2] Ljudsko masno tkivo sadrži oko 87 % lipida.[44]
Postoji stalan tok slobodnih masnih kiselina koje ulaze i izlaze iz masnog tkiva.[2] Smjerom toka upravljaju inzulin i leptin: ako je inzulin povišen, onda postoji ukupan tok prema unutra, a samo kada je razina inzulina niska slobodne masne kiseline mogu napustiti masno tkivo. Izlučivanje inzulina potiče povišena razina šećera u krvi, koja je posljedica konzumiranja ugljikohidrata.[45]
Masne stanice imaju važnu fiziološku ulogu u održavanju razine triglicerida i slobodnih masnih kiselina, kao i određivanju inzulinske rezistencije.[2] Trbušna masnoća ima drugačiji metabolički profil – sklonija je induciranju inzulinske rezistencije. Ovo u velikoj mjeri objašnjava zašto je središnja pretilost marker poremećene tolerancije glukoze i nezavisan čimbenik rizika za kardiovaskularne bolesti (čak i u odsutnosti šećerne bolesti i hipertenzije).[46] Studije ženki majmuna otkrile su da osobe s većim stresom imaju više razine visceralne masnoće. Ovo sugerira moguću uzročno-posljedičnu vezu, pri čemu stres potiče nakupljanje visceralne masnoće, što zauzvrat uzrokuje hormonalne i metaboličke promjene koje pridonose srčanim bolestima i drugim zdravstvenim problemima.[47]
Napredak u biotehnologiji omogućio je prikupljanje matičnih stanica iz masnog tkiva odraslih, što omogućuje stimulaciju ponovnog rasta tkiva upotrebom vlastitih stanica pacijenta. Osim toga, matične stanice dobivene iz masnog tkiva i ljudi i životinja navodno se mogu učinkovito reprogramirati u inducirane pluripotentne matične stanice bez potrebe za fibroblastima.[48] Upotreba vlastitih stanica pacijenta smanjuje mogućnost odbacivanja tkiva i izbjegava etičke probleme povezane s uporabom matičnih stanica ljudskih embrija.[49] Sve veći broj dokaza također sugerira da različite vrste masnih tkiva daju matične stanice različitih osobina.[49][50] Osobine uključuju brzinu rasta, imunofenotip, potencijal diferencijacije, genski izražaj, kao i osjetljivost na uvjete hipoksične kulture:[51] izgleda da razine kisika igraju važnu ulogu u metabolizmu i općenito u funkciji matičnih stanica dobivenih iz masnoga tkiva.[52]
Masno tkivo glavni je periferni izvor aromataze i kod muškaraca i kod žena, pridonoseći proizvodnji estradiola.[53]
Masno tkivo također izlučuje vrstu citokina (stanični signalni proteini) koji se nazivaju adipokini. Oni igraju ulogu u komplikacijama povezanima s pretilošću. Perivaskularno masno tkivo oslobađa adipokine kao što je adiponektin koji utječu na kontraktilnu funkciju krvnih žila koje okružuju.[1][54]
Smeđe masno tkivo[uredi | uredi kôd]

Smeđe masno tkivo (BAT) specijalizirani je oblik masnoga tkiva važan za adaptivnu termogenezu (stvaranje topline po potrebi) kod ljudi i drugih sisavaca. BAT može generirati toplinu "odvajanjem" respiratornog lanca oksidativne fosforilacije unutar mitohondrija putem tkivno-specifične ekspresije razdvajajućeg proteina 1 (UCP1).[55] BAT se prvenstveno nalazi oko vrata i velikih krvnih žila prsnoga koša, gdje može učinkovito sudjelovati u izmjeni topline. BAT se snažno aktivira nakon izlaganja hladnoći otpuštanjem kateholamina iz simpatičkih živaca što rezultira aktivacijom UCP1. Gotovo polovica živaca prisutnih u masnome tkivu senzorni su neuroni povezani s ganglijima dorzalnoga korijena.[56]
Genska osnova[uredi | uredi kôd]
Hipoteza o štedljivom genu ili hipoteza o gladovanju (engleski: thrifty gene hypothesis / famine hypothesis) tvrdi da bi u nekim populacijama tijelo bilo učinkovitije u zadržavanju masnoće u vremenima obilja, pružajući tako veću otpornost na gladovanje u vremenima nestašice hrane. Ovu hipotezu, izvorno iznesenu u kontekstu metabolizma glukoze i inzulinske rezistencije, diskreditirali su fizikalni antropolozi, fiziolozi i sam izvorni zagovornik ideje J. V. Neel u tome kontekstu, iako prema njemu hipoteza ostaje jednako održiva u drugim kontekstima kao i kad je prvi put iznesena.[57][58]
Godine 1995. Jeffrey Friedman s Rudolphom je Leibelom, Douglasom Colemanom i drugima otkrio bjelančevinu leptin koja je nedostajala mišu genski podložnom pretilosti.[59][60][61] Leptin se proizvodi u bijelome masnom tkivu i šalje signale hipotalamusu. Kada razina leptina padne, tijelo to tumači kao gubitak energije, a glad se pojačava. Miševi kojima nedostaje leptin jedu dok ne porastu četiri puta veći od normale.
Leptin, međutim, igra drugačiju ulogu u pretilosti izazvanoj prehranom kod glodavaca i ljudi. Budući da adipociti proizvode leptin, razine leptina kod pretilih su povišene. Međutim, glad ostaje, a kada razina leptina padne zbog gubitka težine glad se povećava. Pad leptina bolje je promatrati kao signal gladovanja nego porast leptina kao signal sitosti. Međutim, povišen leptin kod pretilosti poznat je kao otpornost na leptin. Promjene koje se događaju u hipotalamusu i rezultiraju otpornošću na leptin kod pretilosti u fokusu su istraživanja pretilosti.[62]
Mjerač tjelesne masti[uredi | uredi kôd]
Mjerač tjelesne masti pomagalo je koje se upotrebljava za mjerenje omjera tjelesne masti i težine. Različiti mjerači koriste različite metode za određivanje omjera. Imaju tendenciju očitavanja manjeg postotka tjelesne masti od stvarnoga.
Za razliku od kliničkih alata, jedan relativno jeftin oblik mjerača tjelesne masti koristi princip analize bioelektrične impedancije (BIA). On propušta malu, bezopasnu električnu struju kroz tijelo i mjeri otpor, zatim koristi podatke o težini, visini, dobi i spolu osobe kako bi izračunao približnu vrijednost postotka tjelesne masti osobe. Izračun mjeri ukupnu količinu vode u tijelu (nemasno tkivo i mišići sadrže veći postotak vode od masti) i procjenjuje postotak masti na temelju tih podataka. Rezultat može varirati nekoliko postotaka, ovisno o tome što je pojedeno i koliko je vode popijeno prije analize.
Prije nego što su razvijeni strojevi za analizu bioelektrične impedancije postojalo je mnogo različitih načina za analizu sastava tijela kao što su metode kožnih nabora pomoću pomične mjerke, vaganje pod vodom, pletizmografija istiskivanja zraka cijelog tijela (ADP) i dr.
Izvori[uredi | uredi kôd]
- ↑ a b c Birbrair A, Zhang T, Wang ZM, Messi ML, Enikolopov GN, Mintz A, Delbono O. Kolovoz 2013. Role of pericytes in skeletal muscle regeneration and fat accumulation. Stem Cells and Development. 22 (16): 2298–2314. doi:10.1089/scd.2012.0647. PMC 3730538. PMID 23517218
- ↑ a b c d e f Ye RZ, Richard G, Gévry N, Tchernof A, Carpentier AC. Siječanj 2022. Fat Cell Size: Measurement Methods, Pathophysiological Origins, and Relationships With Metabolic Dysregulations. Endocrine Reviews. 43 (1): 35–60. doi:10.1210/endrev/bnab018
- ↑ Salo. Hrvatski jezični portal. Pristupljeno 6. rujna 2023.
- ↑ Kershaw EE, Flier JS. Lipanj 2004. Adipose tissue as an endocrine organ. The Journal of Clinical Endocrinology and Metabolism. 89 (6): 2548–2556. doi:10.1210/jc.2004-0395. PMID 15181022
- ↑ Mancuso P. Svibanj 2016. The role of adipokines in chronic inflammation. ImmunoTargets and Therapy. 5 (2016): 47–56. doi:10.2147/ITT.S73223. PMC 4970637. PMID 27529061
- ↑ Cannon B, Nedergaard J. Kolovoz 2008. Developmental biology: Neither fat nor flesh. Nature. 454 (7207): 947–948. Bibcode:2008Natur.454..947C. doi:10.1038/454947a. PMID 18719573
- ↑ Aarsland A, Chinkes D, Wolfe RR. Lipanj 1997. Hepatic and whole-body fat synthesis in humans during carbohydrate overfeeding. The American Journal of Clinical Nutrition. 65 (6): 1774–1782. doi:10.1093/ajcn/65.6.1774. PMID 9174472
- ↑ Urbanchek MG, Picken EB, Kalliainen LK, Kuzon WM. Svibanj 2001. Specific force deficit in skeletal muscles of old rats is partially explained by the existence of denervated muscle fibers. The Journals of Gerontology. Series A, Biological Sciences and Medical Sciences. 56 (5): B191–B197. doi:10.1093/gerona/56.5.B191. PMID 11320099
- ↑ Wirth A, Wabitsch M, Hauner H. Listopad 2014. The prevention and treatment of obesity. Deutsches Ärzteblatt International. 111 (42): 705–713. doi:10.3238/arztebl.2014.0705. PMC 4233761. PMID 25385482
- ↑ a b Abdominal fat and what to do about it. President & Fellows of Harvard College. Rujan 2005.
Visceral fat more of a health concern than subcutaneous fat
- ↑ Nagai M, Komiya H, Mori Y, Ohta T, Kasahara Y, Ikeda Y. Svibanj 2010. Estimating visceral fat area by multifrequency bioelectrical impedance. Diabetes Care. 33 (5): 1077–1079. doi:10.2337/dc09-1099. PMC 2858179. PMID 20150289
- ↑ Montague CT, O'Rahilly S. Lipanj 2000. The perils of portliness: causes and consequences of visceral adiposity. Diabetes. 49 (6): 883–888. doi:10.2337/diabetes.49.6.883. PMID 10866038
- ↑ Kern PA, Ranganathan S, Li C, Wood L, Ranganathan G. Svibanj 2001. Adipose tissue tumor necrosis factor and interleukin-6 expression in human obesity and insulin resistance. American Journal of Physiology. Endocrinology and Metabolism. 280 (5): E745–E751. doi:10.1152/ajpendo.2001.280.5.e745. PMID 11287357
- ↑ Marette A. Prosinac 2003. Molecular mechanisms of inflammation in obesity-linked insulin resistance. International Journal of Obesity and Related Metabolic Disorders. 27 (Suppl 3): S46–S48. doi:10.1038/sj.ijo.0802500. PMID 14704744
- ↑ Mokdad AH, Ford ES, Bowman BA, Dietz WH, Vinicor F, Bales VS, Marks JS. Siječanj 2003. Prevalence of obesity, diabetes, and obesity-related health risk factors, 2001. JAMA. 289 (1): 76–79. doi:10.1001/jama.289.1.76. PMID 12503980
- ↑ Maresky HS, Sharfman Z, Ziv-Baran T, Gomori JM, Copel L, Tal S. Studeni 2015. Anthropometric Assessment of Neck Adipose Tissue and Airway Volume Using Multidetector Computed Tomography: An Imaging Approach and Association With Overall Mortality. Medicine. 94 (45): e1991. doi:10.1097/MD.0000000000001991. PMC 4912280. PMID 26559286
- ↑ Brown JC, Harhay MO, Harhay MN. Veljača 2018. Anthropometrically predicted visceral adipose tissue and blood-based biomarkers: a cross-sectional analysis. European Journal of Nutrition. 57 (1): 191–198. doi:10.1007/s00394-016-1308-8. PMC 5513780. PMID 27614626
- ↑ Brown JC, Harhay MO, Harhay MN. Siječanj 2017. Anthropometrically-predicted visceral adipose tissue and mortality among men and women in the third national health and nutrition examination survey (NHANES III). American Journal of Human Biology. 29 (1): e22898. doi:10.1002/ajhb.22898. PMC 5241265. PMID 27427402
- ↑ Reduce Abdominal Fat. Inačica izvorne stranice arhivirana 28. rujna 2011. Pristupljeno 10. travnja 2009..
Estrogen causes fat to be stored around the pelvic region, hips, butt and thighs (pelvic region)
- ↑ Waistline Worries: Turning Apples Back Into Pears. healthywomen.org. Inačica izvorne stranice arhivirana 9. lipnja 2009.
- ↑ Researchers think that the lack of estrogen at menopause plays a role in driving our fat northward. See: A Matter of Fat. Yahoo Health. Women's Health. 1. prosinca 2006. Inačica izvorne stranice arhivirana 15. ožujka 2007.
- ↑ Singh AK, Loscalzo J, ur. 2014. The Brigham Intensive Review of Internal Medicine 2nd izdanje. Oxford University Press. New York, NY. str. 483. ISBN 978-0-19-935827-4. Pristupljeno 3. kolovoza 2021.
- ↑ Ohkawara K, Tanaka S, Miyachi M, Ishikawa-Takata K, Tabata I. Prosinac 2007. A dose-response relation between aerobic exercise and visceral fat reduction: systematic review of clinical trials. International Journal of Obesity. 31 (12): 1786–1797. doi:10.1038/sj.ijo.0803683. PMID 17637702
- ↑ Khalafi M, Malandish A, Rosenkranz SK, Ravasi AA. Rujan 2021. Effect of resistance training with and without caloric restriction on visceral fat: A systemic review and meta-analysis. Obesity Reviews. 22 (9): e13275. doi:10.1111/obr.13275
- ↑ Verheggen RJ, Maessen MF, Green DJ, Hermus AR, Hopman MT, Thijssen DH. Kolovoz 2016. A systematic review and meta-analysis on the effects of exercise training versus hypocaloric diet: distinct effects on body weight and visceral adipose tissue (PDF). Obesity Reviews. 17 (8): 664–690. doi:10.1111/obr.12406. PMID 27213481
- ↑ Irving BA, Davis CK, Brock DW, Weltman JY, Swift D, Barrett EJ, i dr. Studeni 2008. Effect of exercise training intensity on abdominal visceral fat and body composition. Medicine and Science in Sports and Exercise. 40 (11): 1863–1872. doi:10.1249/MSS.0b013e3181801d40. PMC 2730190. PMID 18845966
- ↑ Coker RH, Williams RH, Kortebein PM, Sullivan DH, Evans WJ. Kolovoz 2009. Influence of exercise intensity on abdominal fat and adiponectin in elderly adults. Metabolic Syndrome and Related Disorders. 7 (4): 363–368. doi:10.1089/met.2008.0060. PMC 3135883. PMID 19196080
- ↑ Ross R, Rissanen J. Studeni 1994. Mobilization of visceral and subcutaneous adipose tissue in response to energy restriction and exercise. The American Journal of Clinical Nutrition. 60 (5): 695–703. doi:10.1093/ajcn/60.5.695. PMID 7942575
- ↑ Mazurek T, Zhang L, Zalewski A, Mannion JD, Diehl JT, Arafat H, i dr. Studeni 2003. Human epicardial adipose tissue is a source of inflammatory mediators. Circulation. 108 (20): 2460–2466. doi:10.1161/01.CIR.0000099542.57313.C5. PMID 14581396
- ↑ Pezeshkian M, Noori M, Najjarpour-Jabbari H, Abolfathi A, Darabi M, Darabi M, i dr. Travanj 2009. Fatty acid composition of epicardial and subcutaneous human adipose tissue. Metabolic Syndrome and Related Disorders. 7 (2): 125–131. doi:10.1089/met.2008.0056. PMID 19422139
- ↑ a b Hoehn K, Marieb EN. 2008. Anatomy & Physiology 3rd izdanje. Pearson/Benjamin Cummings. San Francisco, Calif.. ISBN 978-0-8053-0094-9
- ↑ Porter SA, Massaro JM, Hoffmann U, Vasan RS, O'Donnel CJ, Fox CS. Lipanj 2009. Abdominal subcutaneous adipose tissue: a protective fat depot?. Diabetes Care. 32 (6): 1068–1075. doi:10.2337/dc08-2280. PMC 2681034. PMID 19244087
- ↑ Belly fat in women: Taking – and keeping – it off. MayoClinic.com. 8. lipnja 2013. Pristupljeno 2. prosinca 2013.
- ↑ Manolopoulos KN, Karpe F, Frayn KN. Lipanj 2010. Gluteofemoral body fat as a determinant of metabolic health. International Journal of Obesity. 34 (6): 949–959. doi:10.1038/ijo.2009.286. PMID 20065965
- ↑ Devlin MJ, Cloutier AM, Thomas NA, Panus DA, Lotinun S, Pinz I, i dr. Rujan 2010. Caloric restriction leads to high marrow adiposity and low bone mass in growing mice. Journal of Bone and Mineral Research. 25 (9): 2078–2088. doi:10.1002/jbmr.82. PMC 3127399. PMID 20229598
- ↑ Cawthorn WP, Scheller EL, Parlee SD, Pham HA, Learman BS, Redshaw CM, i dr. Veljača 2016. Expansion of Bone Marrow Adipose Tissue During Caloric Restriction Is Associated With Increased Circulating Glucocorticoids and Not With Hypoleptinemia. Endocrinology. 157 (2): 508–521. doi:10.1210/en.2015-1477. PMC 4733126. PMID 26696121
- ↑ Bredella MA, Fazeli PK, Miller KK, Misra M, Torriani M, Thomas BJ, i dr. Lipanj 2009. Increased bone marrow fat in anorexia nervosa. The Journal of Clinical Endocrinology and Metabolism. 94 (6): 2129–2136. doi:10.1210/jc.2008-2532. PMC 2690416. PMID 19318450
- ↑ a b Styner M, Pagnotti GM, McGrath C, Wu X, Sen B, Uzer G, i dr. Kolovoz 2017. Exercise Decreases Marrow Adipose Tissue Through ß-Oxidation in Obese Running Mice. Journal of Bone and Mineral Research. 32 (8): 1692–1702. doi:10.1002/jbmr.3159. PMC 5550355. PMID 28436105
- ↑ Styner M, Pagnotti GM, Galior K, Wu X, Thompson WR, Uzer G, i dr. Kolovoz 2015. Exercise Regulation of Marrow Fat in the Setting of PPARγ Agonist Treatment in Female C57BL/6 Mice. Endocrinology. 156 (8): 2753–2761. doi:10.1210/en.2015-1213. PMC 4511140. PMID 26052898
- ↑ Styner M, Thompson WR, Galior K, Uzer G, Wu X, Kadari S, i dr. Srpanj 2014. Bone marrow fat accumulation accelerated by high fat diet is suppressed by exercise. Bone. 64: 39–46. doi:10.1016/j.bone.2014.03.044. PMC 4041820. PMID 24709686
- ↑ a b Snel M, Jonker JT, Schoones J, Lamb H, de Roos A, Pijl H, i dr. 2012. Ectopic fat and insulin resistance: pathophysiology and effect of diet and lifestyle interventions. International Journal of Endocrinology. 2012: 983814. doi:10.1155/2012/983814. PMC 3366269. PMID 22675355
- ↑ Hens W, Vissers D, Hansen D, Peeters S, Gielen J, Van Gaal L, Taeymans J. Studeni 2017. The effect of diet or exercise on ectopic adiposity in children and adolescents with obesity: a systematic review and meta-analysis. Obesity Reviews. 18 (11): 1310–1322. doi:10.1111/obr.12577. PMID 28913977
- ↑ Hens W, Taeyman J, Cornelis J, Gielen J, Van Gaal L, Vissers D. Lipanj 2016. The Effect of Lifestyle Interventions on Excess Ectopic Fat Deposition Measured by Noninvasive Techniques in Overweight and Obese Adults: A Systematic Review and Meta-Analysis. Journal of Physical Activity and Health. 13 (6): 671–694. doi:10.1123/jpah.2015-0560. PMID 26694194
- ↑ Thomas LW. Travanj 1962. The chemical composition of adipose tissue of man and mice. Quarterly Journal of Experimental Physiology and Cognate Medical Sciences. 47 (2): 179–188. doi:10.1113/expphysiol.1962.sp001589. PMID 13920823
- ↑ Amitani M, Asakawa A, Amitani H, Inui A. 2013. The role of leptin in the control of insulin-glucose axis. Frontiers in Neuroscience. 7: 51. doi:10.3389/fnins.2013.00051. PMC 3619125. PMID 23579596
- ↑ Dhaliwal SS, Welborn TA. Svibanj 2009. Central obesity and multivariable cardiovascular risk as assessed by the Framingham prediction scores. The American Journal of Cardiology. 103 (10): 1403–1407. doi:10.1016/j.amjcard.2008.12.048. PMID 19427436
- ↑ Fat-Bellied Monkeys Suggest Why Stress Sucks. Time. 8. kolovoza 2009. Inačica izvorne stranice arhivirana 20. prosinca 2013. Pristupljeno 19. prosinca 2013.
- ↑ Sugii S, Kida Y, Kawamura T, Suzuki J, Vassena R, Yin YQ, i dr. Veljača 2010. Human and mouse adipose-derived cells support feeder-independent induction of pluripotent stem cells. Proceedings of the National Academy of Sciences of the United States of America. 107 (8): 3558–3563. Bibcode:2010PNAS..107.3558S. doi:10.1073/pnas.0910172106. PMC 2840462. PMID 20133714
- ↑ a b Atzmon G, Yang XM, Muzumdar R, Ma XH, Gabriely I, Barzilai N. Studeni 2002. Differential gene expression between visceral and subcutaneous fat depots. Hormone and Metabolic Research. 34 (11–12): 622–628. doi:10.1055/s-2002-38250. PMID 12660871
- ↑ Baglioni S, Cantini G, Poli G, Francalanci M, Squecco R, Di Franco A, i dr. 4. svibnja 2012. Functional differences in visceral and subcutaneous fat pads originate from differences in the adipose stem cell. PLOS ONE. 7 (5): e36569. Bibcode:2012PLoSO...736569B. doi:10.1371/journal.pone.0036569. PMC 3344924. PMID 22574183
- ↑ Russo V, Yu C, Belliveau P, Hamilton A, Flynn LE. Veljača 2014. Comparison of human adipose-derived stem cells isolated from subcutaneous, omental, and intrathoracic adipose tissue depots for regenerative applications. Stem Cells Translational Medicine. 3 (2): 206–217. doi:10.5966/sctm.2013-0125. PMC 3925056. PMID 24361924
- ↑ Lempesis IG, van Meijel RL, Manolopoulos KN, Goossens GH. Siječanj 2020. Oxygenation of adipose tissue: A human perspective. Acta Physiologica. 228 (1): e13298. doi:10.1111/apha.13298. PMC 6916558. PMID 31077538
- ↑ Stocco C. Siječanj 2012. Tissue physiology and pathology of aromatase. Steroids. 77 (1–2): 27–35. doi:10.1016/j.steroids.2011.10.013. PMC 3286233. PMID 22108547
- ↑ Löhn M, Dubrovska G, Lauterbach B, Luft FC, Gollasch M, Sharma AM. Srpanj 2002. Periadventitial fat releases a vascular relaxing factor. FASEB Journal. 16 (9): 1057–1063. doi:10.1096/fj.02-0024com. PMID 12087067
- ↑ Cannon B, Nedergaard J. Siječanj 2004. Brown adipose tissue: function and physiological significance. Physiological Reviews. 84 (1): 277–359. doi:10.1152/physrev.00015.2003. PMID 14715917
- ↑ Eavesdropping on Communication Between Fat and Brain. 31. kolovoza 2022.
- ↑ Speakerman JR. 2007. Genetics of Obesity: Five Fundamental Problems with the Famine Hypothesis. Fantuzzi G, Mazzone T (ur.). Adipose Tissue and Adipokines in Health and Disease. Nutrition and Health. Humana Press. str. 221–236. doi:10.1007/978-1-59745-370-7_17. ISBN 978-1-58829-721-1
- ↑ Neel JV. 1989. The study of natural selection in primitive and civilized human populations. 1958. Human Biology. 61 (5–6): 781–810, discussion 811–23. PMID 2699601
- ↑ Shell E. 1. siječnja 2002. Chapter 4: On the Cutting Edge. The Hungry Gene: The Inside Story of the Obesity Industry. Atlantic Monthly Press. ISBN 978-1-4223-5243-4
- ↑ Shell E. 1. siječnja 2002. Chapter 5: Hunger. The Hungry Gene: The Inside Story of the Obesity Industry. Atlantic Monthly Press. ISBN 978-1-4223-5243-4
- ↑ Pelleymounter MA, Cullen MJ, Baker MB, Hecht R, Winters D, Boone T, Collins F. Srpanj 1995. Effects of the obese gene product on body weight regulation in ob/ob mice. Science. 269 (5223): 540–543. Bibcode:1995Sci...269..540P. doi:10.1126/science.7624776. PMID 7624776
- ↑ Morris DL, Rui L. Prosinac 2009. Recent advances in understanding leptin signaling and leptin resistance. American Journal of Physiology. Endocrinology and Metabolism. 297 (6): E1247–E1259. doi:10.1152/ajpendo.00274.2009. PMC 2793049. PMID 19724019
