Željezov(III) nitrat
| Željezov(III) nitrat | |

| |
| Strukturna formula | |
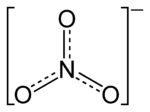 | |
| Svojstva | |
| Sistemsko ime | Željezov(III) nitrat |
| Molekulska formula | Fe(NO3)3 Fe(NO3)3•9H2O (nonahidrat) |
| Molarna masa | 241,86 g/mol (bezvodni) 404,00 g/mol (nonahidrat) |
| Izgled | blijedo ljubičasti kristali |
| CAS broj | 10421-48-4 13476-08-9 (heksahidrat) 7782-61-8 (nonahidrat) |
| Gustoća | 1,68 g/L (bezvodni) |
| Topljivost u vodi | vrlo topljiv (1,5 kg/L) |
| Talište | 47,2 °C (nonahidrat) |
| Vrelište | 125 °C (razgradnja) |
Željezov(III) nitrat, željezova je sol kemijske formule Fe(NO3)3. Budući da je higroskopan, često se nalazi u nonahidratnom obliku, Fe(NO3)3•9H2O), koji je kristalna tvar bezbojne do blijedo ljubičaste boje. Nastaje reakcijom željeza ili željezovih oksida s dušičnom kiselinom.
Svojstva[uredi | uredi kôd]
Vrlo je topljiv u vodi, a topljiv je i u alkoholu i acetonu. Tali se pri 47,2 °C, a razgrađuje se pri 125 °C uz emisiju dušikovih oksida.
Sinteza i proizvodnja[uredi | uredi kôd]
Željezov(III) nitrat kristalizira sa šest ili devet molekula vode iz otopine dobivene otapanjem željeza u dušičnoj kiselini.[1] Kod otapanja željeza treba paziti na koncentraciju upotrebljene kiseline. Ako je kiselina previše razrijeđena nastaje željezov(II) nitrat, a ako je previše koncentrirana, željezo postaje pasivno.
- Fe + 4HNO3 → Fe(NO3)3 + 2H2O + NO↑
Uporaba[uredi | uredi kôd]
Željezov(III) nitrat koristi se kao katalizator za sintezu natrijevog amida iz otopine natrija u amonijaku
- 2 NH3 + 2 Na → 2 NaNH2 + H2↑
Određene gline impregnirane željezovim(III) nitratom koriste se kao kao oksidans u organskoj sintezi. Npr. željezov(III) nitrat na montmorilonitskom reagensu zvanom "Clayfen" korišten je za oksidaciju alkohola u aldehide i tiola u disulfide.[2]
Otopina željezovog(III) nitrata koristi se u metalurgiji i draguljarstvu za graviranje srebra i njegovih slitina.
Izvori[uredi | uredi kôd]
- ↑ I. Filipović, S. Lipanović: Opća i anorganska kemija, II dio: Kemijski elementi i njihovi spojevi, Školska knjiga, Zagreb, 1991, str. 1033.
- ↑ Cornélis, A. Laszlo, P.; Zettler, M. W. "Iron(III) Nitrate–K10 Montmorillonite Clay" in Encyclopedia of Reagents for Organic Synthesis (Ed: L. Paquette) 2004, J. Wiley & Sons, New York. DOI: 10.1002/047084289.
