Beta-oksidacija
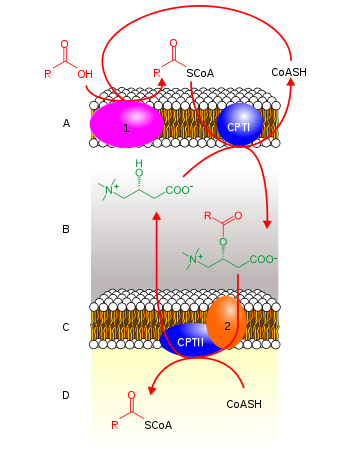
crveno: acil-CoA, zeleno: karnitin, crveno+zeleno: acil karnitin, CoASH: koenzim A, CPTI: karnitin aciltransferaza I, CPTII: karnitin aciltransferaza II, 1: acil-CoA sintetaza, 2: translokaza, A: vanjska mitohondrijska membrana, B: međumembranski prostor, C: unutarnja mitohondrijska membrana, D: mitohondrijski matriks
Beta-oksidacija je kružni metabolički proces kojim se masne kiseline, prethodno modificirane u oblik acil-koenzima A (Acil-CoA), postepeno razgrađuju do konačnog produkta Acetil-CoA. Acetil-CoA ulazi potom u Krebsov ciklus kao početna molekula. Beta-oksidacija odvija se u mitohondrijima i/ili peroksisomima u četiri metabolička prijelaza koji se ponavljaju, s određenim razlikama pri razgradnji nezasićenih masnih kiselina i masnih kiselina s neparnim brojem ugljikovih atoma.
Masne kiseline moraju proći tri metabolička koraka da bi mogle biti razgrađene u Acetil-CoA:
1. Aktivacija masnih kiselina u citosolu
2. Prijenos masnih kiselina iz citosola u mitohondrij (prijenos karnitina)
3. Beta-oksidacija u matriksu mitohondrija
Većina tkiva oksidira masne kiseline kao metaboličko gorivo, s izuzetkom mozga koji ih vrlo teško koristi i eritrocita i moždine nadbubrežne žlijezde koja ih ne može koristiti. Kod nekih je životinja beta-oksidacija posebno korisna za dobivanje energije tijekom zimskog sna (hibernacije), dok neke pustinjske životinje dobivaju vodu razgradnjom masnih kiselina. Biljke pak vrše beta-oksidaciju u peroksisomima listova i sjemena, koja nema ulogu proizvodnje energije već stvaranja prekursora za druge biosintetske reakcije.
Koraci koji prethode beta-oksidaciji[uredi | uredi kôd]
Aktivacija masnih kiselina[uredi | uredi kôd]
Slobodne masne kiseline s lakoćom prolaze staničnu membranu u citosol, jer su vrlo hidrofobne molekule. Aktivaciju masnih kiselina u citosolu katalizira enzim acil CoA sintetaza. Masne kiseline reagiraju s ATP i nastaju acil adenilat i anorganski pirofosfat (PPi). Acil adenilat reagira potom s koenzimom A i kao produkt nastaje acil-koenzim A i AMP. Stehiometrijska reakcija aktivacije masnih kiselina:
R–COOH + ATP + CoASH → R–CO–SCoA + AMP + PPi + H2O
Prijenos acil-CoA u mitohondrij[uredi | uredi kôd]
Radi njegove hidrofilne prirode, Acil-CoA ne može spotano proći iz citosola kroz mitohondrijske membrane do matriksa. Acil-CoA stoga reagira s karnitinom i formira acil karnitin, koji se prenosi kroz obje membrane u matriks mitohondrija.
Proces prijenosa acil karnitina odvija se u tri faze:
1. Enzim karnitin aciltransferaza I ili karnitin palmitoiltransferaza I (CPTI), koji se nalazi na vanjskoj mitohondrijskoj membrani, odstranjuje koenzim A iz acil-CoA i veže acilnu skupinu na karnitin formirajući tako acil karnitin. Koenzim A se oslobađa u citosol i može biti iskorišten za aktivaciju sljedeće masne kiseline.
2. Transportna bjelančevina translokaza, koja se nalazi na unutarnjoj mitohondrijskoj membrani, prebacuje acil karnitin u matriks.
3. Enzim karnitin acitransfraza II ili karnitin palmitoiltransferaza II (CPTII), koji je tijesno vezan za translokazu, oslobađa molekulu karnitina od acilne skupine i ponovo je veže za koenzim A. Oslobođeni karnitin se prenosi izvan mitohondrija, kao bi mogao ponoviti ciklus.
Aktivnost prijenosa Acil CoA u mitohondrij inhibirana je od strane malonil-CoA, jednog od ključnih regulatora metabolizma masnih kiselina.
Beta-oksidacija kao kružni proces u četiri stupnja[uredi | uredi kôd]
Unutar mitohondrija, svaki se ciklus beta-oksidacije sastoji od niza četiriju reakcija u kojima se razgradnjom acil-CoA oslobađa jedna molekula acetil-CoA[1]:
| Opis | Kemijska reakcija | Enzim | Konačni produkt |
| Dehidrogenacija FAD-om: Prvi je korak oksidacija masne kiseline od strane enzima acil-CoA dehidrogenaze, koji katalizira formiranje dvostruke veze između C2 i C3. |  |
acil CoA dehidrogenaza | trans-Δ2-enoil-CoA |
| Hidratacija: Drugi je korak hidratacija dvostruke veze između C2 i C3. Ova je reakcija stereospecifična, i dopušta formiranje samo L-izomera. |  |
enoil CoA hidrataza | L-β-hidroksiacil-CoA |
| Oksidacija NAD+-om: Treći je korak oksidacija L-β-hidroksiacil-CoA od strane NAD+, pri čemu se hidroksilna skupina konvertira u ketonsku skupinu. |  |
L-β-hidroksiacil CoA dehidrogenaza | β-ketoacil-CoA |
| Tioliza: Posljednji je korak odvajanje β-ketoacil CoA, tiolnom skupinom koja pripada drugoj molekuli koenzima A. Tiol je umetnut između C2 i C3. |  |
tiolaza (acil-CoA acetiltransferaza) | acetil-CoA i acil-CoA, koji je kraći za dva atoma ugljika |
Ovaj se proces u četiri koraka ponavlja dok se cijeli lanac ne razgradi u molekule acetil-CoA. U posljednjem se ciklusu formiraju dvije molekule acetil-CoA, umjesto jedne acil-CoA i jedne acetil-CoA.
Multienzimski kompleks[uredi | uredi kôd]
Enzimi koji kataliziraju zadnja tri stupnja beta-oksidacije povezani su u veliki multienzimski sklop, koji se nalazi na unutarnjoj membrani mitohondrija i naziva se trifunkcijski enzim (TFP). Ovaj enzimski sklop je heterooktamer, tj. izgrađen je od četiri α i četiri β podjedinice. Podjedinice α se funkcionalno podudaraju s enoil-CoA hidratazom i L-β-hidroksiacil-CoA-dehidrogenazom, dok podjedinice β vrše aktivnost tiolaze. Bliska interakcija ovih enzima uvelike ubrzava cijeli metabolički proces i čini ga učinkovitijim, pošto se substrati ne disociraju od samih enzima pri prijelazu na sljedeću reakciju.
Beta-oksidacija nezasićenih masnih kiselina[uredi | uredi kôd]
Opisane reakcije beta-oksidacije vrijede samo za degradaciju zasićenih masnih kiselina u kojima su atomi ugljika vezani jednostrukim kovalentnim vezama. Kod nezasićenih masnih kiselina, prisutnost jedne ili više dvostrukih kovalentnih veza među atomima ugljika u cis poziciji, sprječava formiranje trans-Δ2-enoil-CoA. Pri razgradnji nezasićenih masnih kiselina, u reakciju stupaju dva dodatna enzima.
- Kod nezasićenih masnih kiselina s jednom dvostrukom vezom, kao npr. oleinska kiselina C18:1(Δ9), enzim Δ3,Δ2-enoil-CoA izomeraza katalizira izomerizaciju cis-Δ3-enoil-CoA u trans-Δ2-enoil-CoA, koji je uobičajeni substrat beta-oksidacije. Daljnje se reakcije odvijaju uobičajenim tijekom.
- Kod nezasićenih masnih kiselina s dvije ili više dvostrukih veza, kao npr. linolna kislina - C18:2(Δ9,12), gore navedena izomeraza najprije katalizira izomerizaciju cis pozicije u trans. Potom enzim 2,4-dienoil-CoA-reduktaza reducira dvostruku vezu u jednostruku, pri čemu se koristi reducirani nikotinamid adenin dinukleotid fosfat (NADPH + H+) kao donor vodika. Potom enoil-CoA-izomeraza katalizira izomerizaciju cis u trans. Ostale se reakcije odvijaju uobičajenim tijekom.
Beta-oksidacija masnih kiselina s neparnim brojem ugljikovih atoma[uredi | uredi kôd]
Većna prirodnih lipida sadrži masne kiseline s parnim brojem ugljikovih atoma, ali neke biljke i morski organizmi mogu sadržati i masne kiseline s neparnim brojem C atoma. Ovi lanci masnih kiselina bivaju oksidirani uobičajenim metaboličkim putem do posljednjeg niza reakcija, pri čemu ne nastaju dva acetil-CoA već jedan acetil-CoA i jedan propionil-CoA. Propionil-CoA razgrađuju tri dodatna enzima.
- Propionil CoA carboksilaza katalizira reakciju karboksilacije (vezivanja CO2), pri čemu nastaje D-metilmalonil-CoA. Kofaktor enzima je biotin (vitamin H) koji aktivira bikarbonatni ion HCO3-, a energiju za samu reakciju daje ATP:
propionil-CoA + HCO3- + ATP → D-metilmalonil-CoA + ADP + Pi
- Metilmalonil-CoA epimeraza potom pretvara D-izomer u L-metilmalonil-CoA. Ova reakcija zahtijeva 5'-deoksiadenozilkobalamin ili vitamin B12 kao kofaktor.
- Metilmalonil-CoA mutaza katalizira pretvorbu L-metilmalonil-CoA u sukcinil CoA.
Sukcinil CoA može ući u Krebsov ciklus kao međuspoj.
Beta-oksidacija u peroksisomima[uredi | uredi kôd]

Osim u mitohondrijima, beta-oksidacija može se dovijati i u peroksisomima kad je duljina lanaca masnih kiselina vrlo velika. Kod peroksisomske beta-oksidacije, proces ne razgrađuje u potpunosti lanac masne kiseline, već se zaustavlja na oktanilu-CoA.
Postoji nekoliko bitnih razlika između mitohondrijske i peroksisomske beta-oksidacije, koja zahtijeva i različite enzime.
Aktivirane masne kiseline prenosi posebna peroksisomalna karnitin acil transferaza (umjesto uobičajene acil transferaze I i II).
Unutar peroksisoma, aktivirane masne kiseline (acil-CoA) oksidira prvi enzim flavoprotein acil-CoA oksidaza koja katalizira nastanak dvostruke veze po sljedećoj formuli:
acil-CoA + O2 trans-2,3-dehidroacil-CoA + H2O2
Za napomenuti je da ova reakcija oksidacije nije vezana za proizvodnju ATP. Pri peroksisomnoj beta-oksidaciji akceptori elektrona nisu NAD i FAD, već molekula kisika (O2), koja redukcijom prelazi u vodikov peroksid (H2O2), tako da se većina energije u stvari gubi u obliku topline. Pošto je vrlo toksičan za stanicu, vodikov peroksid vrlo brzo razgrađuje enzim katalaza.
Drugu reakciju odvajanja acetila CoA od preostalog acil CoA katalizira enzim β-ketotiolaza, koja je po afinitetu prema substratima razičita od mitohondrijske tiolaze.
Beta-oksidacija je vrlo važan metabolički proces kod biljnih stanica. Biljke ne koriste ovaj proces za dobivanje energije, već za sintezu bitnih metaboličkih spojeva kao glukoze, saharoze i dr. Beta-oksidacija kod biljaka najviše se odvija u stanicama listova i u sjemenu u organelima koji se u ovom slučaju nazivaju glioksisomi.
Beta-oksidacija kod životinja[uredi | uredi kôd]

Za vrijeme hibernacije i kod dugih seoba, neke životinje jako ovise o energetskim rezervama u masnom tkivu. Beta-oksidacija postaje osnovni proces dobivanja energije za vrijeme zimskog sna, koje životinje kao npr. medvjed ili puh, koriste za proizvodnju topline, anaboličke procese i membranski transport.
Tijekom beta-oksidacije oslobađaju se i velike količine vode, koja može zamijeniti izgubljenu količinu vode disanjem ili transpiracijom prilikom znojenja u izuzetno vrućem i suhom okolišu. kod potpune razgradnje jedne molekule masne kiseline npr. palmitinske kiseline moguće je dobiti 23 molekule vode. Najpoznatiji primjer takve prilagodbe su deve, koje imaju velike rezerve masti pohranjene u leđnim grbama. Deve razgrađuju mast iz grba kako bi dobile vodu, što im omogućava preživljavanje u pustinjskom ambijentu, bez potrebe za čestim pristupom izvorima vode.
Izvori[uredi | uredi kôd]
- ↑ Nelson, D. L. & Cox, M. M. (2005). Lehninger Principles of Biochemistry, 4. izdanje. New York: W. H. Freeman and Company, ISBN 0-7167-4339-6.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

