Mliječna kiselina
| Mliječna kiselina C3H6O3 | ||||||||
|---|---|---|---|---|---|---|---|---|
 | ||||||||
| IUPAC nomenklatura | {{{IUPAC nomenklatura}}} | |||||||
| Ostala imena | {{{ostala imena}}} | |||||||
| Identifikacijski brojevi | ||||||||
| CAS broj | 50-21-5 ✓ | |||||||
| EC broj | 200-018-0 ✓ | |||||||
| PubChem broj | 612 ✓ | |||||||
| Osnovna svojstva | ||||||||
| Molarna masa | {{{molarna masa}}} | |||||||
| Izgled | {{{izgled}}} | |||||||
| Struktura | ||||||||
| Sigurnosne upute | ||||||||
| ||||||||
| Međunarodni sustav mjernih jedinica primijenjen je gdje god je to bilo moguće. Ako nije drugačije naznačeno, upisane vrijednosti izmjerene su pri standardnim uvjetima. | ||||||||
| Portal:Kemija | ||||||||
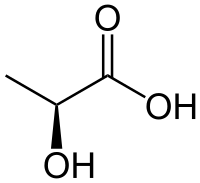
Mliječna kiselina uobičajeno je ime za alfa-hidroksi-karboksilnu kiselinu, odnosno 2-hidroksipropionsku kiselinu, CH3CH(OH)COOH.[1] Pripada skupini hidroksikarboksilnih kiselina.
U svojoj molekuli sadrži jedan asimetrični ugljikov atom pa se pojavljuje u dvjema optički aktivnim modifikacijama (D-mliječna i L-mliječna kiselina) te kao njihova racemična, optički neaktivna smjesa (DL-mliječna kiselina). Tvori bezbojne kristale koji se tale na 25 do 26 °C (D-m. k. i L-m. k.), odnosno na 18 °C (DL-m.k.), pa prelaze u bezbojnu sirupastu higroskopnu tekućinu, vrlo lako topljivu u vodi i alkoholu, teško topljivu u eteru.[2]
L-mliječna kiselina stvara se raspadanjem glikogena u mišićima koji su pod opterećenjem. D-mliječna kiselina nastaje vrenjem iz šećera i drugih ugljikohidrata djelovanjem anaerobnih bakterija, pa se zato nalazi u kiselome mlijeku, kiselom zelju, siru, siliranom krmivu itd. Mliječna kiselina industrijski se proizvodi fermentacijom šećera iz škroba, melase ili sulfitne lužine, a sintetski reakcijom cijanovodične kiseline i acetaldehida, uz kiselinski nitril kao međuproizvod. Rabi se umjesto limunske i vinske kiseline u proizvodnji bezalkoholnih pića, kiselih bombona, u medicini, tekstilnoj i kožnoj industriji, industriji vrenja i dr. I mnoge soli i esteri mliječne kiseline (laktati) važni su u tehnici i medicini. Tako su npr. natrijev laktat i kalijev laktat nadomjesci za glicerol. Magnezijev laktat blagi je laksativ, etil-laktat hipnotik je i sedativ, a u tehnici služi kao otapalo, titanijev laktat služi za močenje kože itd.[2]
U vinarstvu se ponekad ubraja u nehlapljive kiseline. Vinu daje harmoničnost i pitkost. Poželjna u vinu, do određene granice. Prelazak dopustivog praga hlapljivih kiselina javlja se ako se vino dobilo od nezrelog grožđa, vino se onda mora ponekad otkiseliti. Ako su berbe bile nepovoljne, grožđe je nezrelo pa odgađamo prvi pretok. Tada bakterije i kvasci koje su na drožđu same razgrade jabučnu kiselinu u blagu mliječnu kiselinu (jabučno-mliječno vrenje) te vino postaje mekše i pitkije.[3]
Izvori[uredi | uredi kôd]
- ↑ Mliječna kiselina. Hrvatsko strukovno nazivlje – Struna. Pristupljeno 8. svibnja 2022.
- ↑ a b Mliječna kiselina. Hrvatska enciklopedija. Pristupljeno 8. svibnja 2022.
- ↑ Prvi hrvatski vinogradarski portal Nenad Bižić: Pretok i bistrenje vina (pristupljeno 1. studenoga 2015.)


