Johannes Rydberg
| Johannes Rydberg | |
 | |
| Rođenje | 8. studenog 1854. Halmstad, Švedska |
|---|---|
| Smrt | 28. prosinca 1919. Lund, Švedska |
| Državljanstvo | Šveđanin |
| Polje | Fizika |
| Institucija | Institut za fiziku u Lundu |
| Alma mater | Sveučilište u Lundu |
| Poznat po | Rydbergova formula Rydbergova konstanta |
| Istaknute nagrade | član Kraljevskog društva (1919.) |
| Portal o životopisima | |
Johannes Rydberg, punim imenom Johannes Robert Rydberg (Halmstad, 8. studeni 1854. – Lund, 28. prosinac 1919.), švedski fizičar i astronom. Studirao u Lundu, gdje je i doktorirao matematiku 1879. Od 1901. bio je profesor u Institutu za fiziku u Lundu. Bavio se proučavanjem optičkih spektara. Prvi je uočio da se valni brojevi atomskih spektara svih kemijskih elemenata dadu prikazati kao umnožak dvaju faktora, od kojih je jedan promjenjiv (varijabilan), a drugi stalan (konstantan). Taj konstantni faktor dobio je naziv Rydbergova konstanta. Bohrova je teorija, međutim, pokazala, a poslije su točnija mjerenja to i potvrdila, da se Rydbergova konstanta ponešto razlikuje od kemijskog elementa do kemijskog elementa i da je njezina prava vrijednost R za dani element:
gdje je: m - masa elektrona, M+ - masa jednostruko ioniziranog atoma dotičnog elementa, a R∞ - univerzalna Rydbergova konstanta, to jest:
gdje je: e - električni naboj elektrona, c - brzina svjetlosti, h - Planckova konstanta.
Bio je član Kraljevskog društva (eng. Royal Society) od 1919. Po njem su nazvani krater na Mjesecu (Rydberg (krater)) i planetoid (10506 Rydberg).[1] Pobuđeni atomi, s vrlo visokim kvantnim brojevima, a koje predstavlja broj n u Rydbergovoj formuli, nazivaju se Rydbergovi atomi. Rydbergova predviđanja da će vodikove spektralne linije, koja se dobiju iz Rydbergove formule, pomoći u teoretskom razumijevanju atomske strukture, iskoristio je 1913. N. Bohr i stvorio Bohrov model atoma. U spektroskopiji se koristi konstanta, koja se zasniva na teoretskom atomu beskonačne mase, i naziva se Rydberg (R) u njegovu čast.
Iskustvene činjenice o spektrima[uredi | uredi kôd]









Užarena čvrsta tijela emitiraju svjetlost s kontinuirano raspodijeljenim valnim duljinama (toplinsko zračenje). Od temperature užarenog tijela zavisi koji je dio spektra najjači (najintenzivniji), ali od mjesta maksimuma postepeno se gasi svjetlost prema manjim i većim valnim duljinama. Nasuprot tome kontinuiranom spektru čvrstih tijela opaža se kod plinova i para nešto drugo. U njihovu se spektru pojavljuju diskretne linije, koje su svojstvene za pojedine kemijske elemente. Čitav spektar se sastoji od niza oštro određenih linija.
Lako je uvidjeti da linijski spektar potječe od atoma. Takvi se spektri dobivaju pri pokusima s katodnim i kanalnim zrakama. Električno izbijanje u katodnoj cijevi niskog tlaka izaziva uvijek velik broj atoma na emisiju svjetlosti. Linijske spektre emitiraju također i plemeniti plinovi, koji se sastoje od čistih atoma, a ne molekula.
Linijske spektre možemo studirati na emisijskom ili apsorpcijskom spektru. Pusti li se bijela svjetlost kroz neke pare ili plin, opaža se u dobivenom spektru da su neke valne duljine ugušene. Tamne linije stoje točno na onim mjestima spektra gdje bi ležale emisijske linije. Plin dakle apsorbira svjetlost onih valnih duljina koje bi inače emitirao. Apsorpcijski spektar slaže se potpuno s emisijskim. Ova određenost u spektrima kemijskih elemenata jedan je od temeljnih zakona nuklearne fizike.
Iako svakom kemijskom elementu pripadaju posebne, svojstvene spektralne linije, ipak se u njihovim spektrima opažaju neka zajednička svojstva, koja omogućuju da se unese red u golem spektroskopski materijal. Spektralne linije svakog kemijskog elementa daju se srediti u nekoliko serija. Svaka pojedina serija predstavlja niz linija koje su poredane po određenom pravilu. Često se već na prvi pogled vidi da linije jedne serije pripadaju zajedno. Promatramo li linije od većih valnih duljina prema manjim, udara nam odmah u oči da se razmak između njih smanjuje. Linije se gomilaju prema određenoj valnoj duljine, koja je granica te serije.
Prvi je J. J. Balmer 1885. otkrio da se vodikov spektar može prikazati jednostavnom matematičkom jednadžbom. Njemu su tada bile poznate 4 vidljive vodikove linije s valnim duljinama:
- Hα = 656, 199 nm
- Hβ = 486, 152 nm
- Hγ = 434, 067 nm
- Hδ = 410, 194 nm
Običaj je da se vodikove linije označe početnim slovima grčkog alfabeta, koja dolaze kao indeksi kemijskom simbolu H. Recipročne vrijednosti valnih duljina tih četiriju linija daje se jednadžbom (Rydbergova formula):
gdje je: m = 3, 4, 5, 6; a R je takozvana Rydbergova konstanta. Uvrstimo li u Balmerovoj jednadžbi za m cijele brojeve veće od 7 dobivamo valne duljine koje leže u ultraljubičastom području spektra. Pokusima se doista našlo još oko 30 linija koje se potpuno slažu s Balmerovom jednadžbom. Linije se gomilaju prema valnoj duljini koja je dana izrazom:
To je granica serije. Balmerova serija je idealni tip spektralnih linija uopće. Kako se vidi na slici, razmak između susjednih linija pravilno se smanjuje, i linije se gomilaju prema određenoj granici.
Iz razloga koji će se kasnije iznijeti uvedeno je da se spektralne jednadžbe postavljaju za frekvencije, a ne za valne duljine. Pokusima se, doduše, mjere valne duljine (iz interferentnih, ogibnih ili disperzionih pojava), ali zakoni spektralne analize postaju pregledniji kad se uzimaju u obzir frekvencije. Pri tom treba misliti na sljedeće: frekvencija ν se može izračunati iz valne duljine λ prema poznatom odnosu:
No brzina svjetlosti c nije tako točno izmjerena kako su točna mjerenja valne duljine. Točnost spektralne analize je nenadmašiva. Iz tog razloga i dalje se u spektralnoj analizi svi iskustveni podaci izražavaju u valnim duljinama.
Uvodeći frekvenciju, možemo Balmerovu jednadžbu pisati u obliku:
gdje je m = 3, 4, 5…. Frekvencije spektralnih linija vodika mogu se dakle prikazati kao razlike (diferencije) između dva člana, od kojih je prvi konstantan, a drugi opada kao 1/9, 1/16, 1/25, 1/36 …. Tu se odmah nameće pitanje: Mora li se uvijek uzeti kao konstantan broj 1/4? Moguće je pomisliti, da prvi konstantni član bude bilo koji razlomak 1/n2. Godine 1908. našao je F. Paschen u infracrvenom području spektralne linije vodika kojima su se valne duljine točno slagale s izrazima:
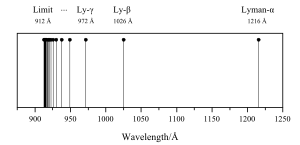
Tu dakle imamo dva člana jedne serije, kojoj je konstantni član R/32. Taj član ujedno određuje i granicu serije. I od te takozvane Paschenove serije nađen je vrlo velik broj linija. Godine 1916. pronašao je Lyman na drugoj strani od Balmerove serije, duboko u ultraljubičastom području, nove spektralne linije, koje smo mogli prikazati istom Balmerovovom jednadžbom, samo što je za konstantni član trebalo uzeti u nazivniku cijeli broj 1. Vodikov spektar sastoji se, od ovih serija:
Lymanova serija:
gdje je: m = 2, 3, 4 ….
gdje je: m = 3, 4, 5 ….
Paschenova serija:
gdje je: m = 4, 5, 6 ….
Brackettova serija:
gdje je: m = 5, 6, 7 ….
Pfundova serija:
gdje je: m = 6, 7, 8 ….
Od tog golemog mnoštva linija padaju u vidljivo područje spektra svega prve 4 linije Balmerove serije. Odatle se vidi kako je važno ispitivati čitav spektar da se nađu osnovni zakoni serije.
Frekvencije spektralnih linija vodika možemo općenito izraziti jednadžbom:
gdje su: n i m - cijeli brojevi.
Frekvencije vodikovih linija dobiju se, dakle, da se od niza c∙R/n2 učine sve moguće pozitivne razlike (diferencije). Tako objašnjena, Balmerova jednadžba vodi nas do općeg načela kombinacije, što ga je otkrio W. Ritz 1908. Po tom načelu dade se za svaki kemijski element postaviti niz terma T1, T2, T3, …. tako da su frekvencije njegova spektra dane razlikama (diferencijama):
Ritzovo načelo kombinacije potvrđeno je pri ispitivanju svih spektara. Ono je ključ za sređivanje različitih serija. Načelo kombinacije sadrži u sebi osnovni zakon prirode, koji se u punom smislu razotkriva tek u nuklearnoj fizici.[2]
Izvori[uredi | uredi kôd]
- ↑ Rydberg, Johannes Robert , [1] "Hrvatska enciklopedi-ja", Leksikografski zavod Miroslav Krleža, enciklopedija.hr, 2017.
- ↑ Ivan Supek: "Nova fizika", Školska knjiga Zagreb, 1966.
- Mike Sutton, “Getting the numbers right – the lonely struggle of Rydberg” Chemistry World, Vol. 1, No. 7, July 2004.
- Martinson Indrek, L.J. Curtis: "Janne Rydberg – his life and work", journal = NIM B, [2] 2005.
- O'Connor, John J.; Robertson, Edmund F., "Johannes Rydberg", MacTutor History of Mathematics archive, University of St Andrews, [3] .















