Atom







Atom (grč. ἄτομος: nedjeljiv) je osnovni djelić, najmanji dio na koji kemijska tvar može biti rastavljena bez otpuštanja električki nabijenih čestica (elektrona), najmanji sastavni dio najjednostavnijih kemijskih tvari, kemijskih elemenata, koji zadržava svojstva tog elementa. Promjer atoma iznosi od 0,1 do 0,5 nanometara, a relativna atomska masa od oko 1 za vodik do približno 244 za plutonij. Atomi su dovoljno maleni da pokazuju i valna svojstva, na primjer valna duljina vodikovih atoma na sobnoj temperaturi iznosi oko 0,1 nm, a cezijevih 0,01 nm. Zornu sliku atoma nemoguće je predočiti svakodnevnim makroskopskim pojmovima. Potpun opis daje kvantna mehanika sa zamisli (konceptom) kvantiziranosti stanja i vjerojatnošću nalaženja elementarnih čestica u pojedinim stanjima.[1]
U atomskoj teoriji materije, atom se sastoji od atomske jezgre oko koje kruže elektroni (elektronski omotač atoma). Danas je općenito priznato mišljenje da se atomska jezgra svih kemijskih elemenata sastoji od pozitivno nabijenih protona i neutrona koji nemaju električni naboj. Čestice koje se nalaze u atomskoj jezgri, to jest protoni i neutroni, zovu se zajedničkim imenom nukleoni (lat. nucleus: jezgra). Neutron ima masu gotovo jednaku masi protona. Proton je jezgra vodikovog atoma, pa mu je masa jednaka masi atoma vodika. Broj protona u atomskoj jezgri koji se zove atomski broj, jednak je njezinom električnom naboju i uvijek odgovara rednom broju kemijskog elementa u periodnom sustavu. Dakle atomskim brojem određena je vrsta kemijskog elementa.
U neutralnom atomu broj elektrona što kruže oko jezgre jednak je broju protona u jezgri. Pozitivan naboj jednog protona jednako je velik kao negativan naboj elektrona. 1869. ruski kemičar D. I. Mendeljejev otkrio je zakonitost ponavljanja kemijskih svojstva elemenata kod povećanja njihove atomske mase. On je tada sve poznate elemente poredao po rastućim atomskim masama jedan iznad drugoga i sastavio periodičku tablicu. Mendeljejev je dokazao da svaki kemijski element ima određen sastav atoma koji označuje atomska masa i mjesto u periodnom sustavu elemenata.[2]
Jezgra čini 99,99% mase atoma. Međutim, ako bi se atom uvećao toliko da jezgra bude promjera jabuke, a elektroni veličine bobice grožđa, promjer atoma bi bio 1 kilometar. Dakle, većinu atoma zauzima prazan prostor. Promjer jezgre (10-15 m) je 100 000 puta manji od promjera atoma (10-10 m).
Građa atoma[uredi | uredi kôd]
Atomi se sastoje od atomske jezgre i elektronskog omotača. Jezgra se nalazi u središtu atoma i čini 99,9% njegove mase, a zauzima samo oko 10–14 volumena atoma. Na primjer kada bi atom bio kugla promjera 6 kilometara, jezgra bi bila veličine teniske loptice. Svi sastavni dijelovi u atomu u neprestanu su gibanju.
Atomska jezgra[uredi | uredi kôd]
Atomska jezgra se sastoji od električki pozitivno nabijenih protona i neutralnih neutrona. Promjera je od 1,75 · 10–15 m (vodikova jezgra) do 15 · 10–15 m (uranijeva jezgra). Protoni i neutroni su u jezgri stopljeni zajedno djelovanjem privlačne nuklearne, odnosno jake sile. Protoni i neutroni sastavljeni su od triju još manjih čestica, kvarkova.
Elektronski omotač[uredi | uredi kôd]
Elektronski omotač tvore električki negativno nabijeni elektroni kojima je masa 1836 (1839) puta manja od mase protona (neutrona). Negativno nabijene elektrone elektromagnetskom silom privlači pozitivno nabijena jezgra, no oni posjeduju dovoljno energije da se, zbog kvantnih učinaka, uspijevaju zadržati na određenoj udaljenosti od jezgre, raspoređeni u ljuske. Energija je elektrona kvantizirana, može poprimiti samo određene vrijednosti (kvant energije). Svako energijsko stanje elektrona karakterizirano je četirima kvantnim brojevima. Glavni kvantni broj n određuje ljusku kojoj elektroni pripadaju i ima vrijednosti od 1 do 7. Elektroni s najmanje energije najbliže su jezgri i popunjavaju prvu ljusku, koja se označuje slovom K. Sljedeće su ljuske L, M, N, O, P i Q. Za svaku ljusku svojstven je broj elektrona koje ona može sadržati (2∙n2). Ljuska K može sadržati samo dva elektrona, ljuska L 8, ljuska M 18, ljuska N 32. Vanjske ljuske O, P, i Q nisu nikad u potpunosti popunjene, no zna se da teorijski mogu sadržati 50, 72 odnosno 98 elektrona (atomska struktura). Broj protona u atomu jednak je broju elektrona, što čini atom neutralnim.
Vrste atoma[uredi | uredi kôd]
Broj protona najvažnije je svojstvo atoma, njime je određen i broj elektrona i kemijska svojstva atoma; naziva se atomski broj (oznaka Z). Dosad je otkriveno 112 različitih atoma koji su prema svojem atomskom broju razvrstani u periodni sustav elemenata. Na prvom je mjestu vodik s jednim protonom i atomskim brojem 1. Uranij s brojem 92 i plutonij s brojem 94 posljednji su u nizu koji se mogu naći u prirodi, atomi s većim brojem protona se proizvode (na primjer u akceleratoru teških iona GSI Helmholtzzentrum für Schwerionenforschung, Darmstadt, Njemačka). Na primjer atom s brojem 112 (kopernicij) dobiven je 1996. nuklearnom fuzijom cinka i olova. Atomi s velikim atomskim brojem nestabilni su, na primjer vrijeme poluraspada kopernicija (283 112 Cn) je samo 4 sekunde.
Izotopi[uredi | uredi kôd]
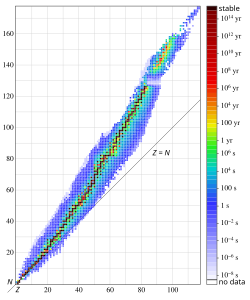
Atomi jednog kemijskog elementa mogu se razlikovati po broju neutrona u jezgri. Lakši atomi imaju približno jednak broj protona i neutrona, dok teži atomi imaju više neutrona. Atomi koji imaju jednak broj protona a različit broj neutrona nazivaju se izotopi. Na primjer vodik ima još dva izotopa, deuterij i tricij. Gotovo svi elementi imaju po nekoliko izotopa. Poznato je 287 prirodnih izotopa, a umjetno ih je proizvedeno mnogo više. Atom može dobiti ili izgubiti elektron, ili više njih, i tada se naziva negativnim ili pozitivnim ionom. Međudjelovanje atoma i njihov odgovor na elektromagnetsko zračenje ovise o strukturi elektrona oko jezgre. Elektroni u atomu mogu apsorpcijom ili emisijom elektromagnetskoga zračenja prelaziti iz jednoga kvantnog stanja u drugo. To daje emisijski ili apsorpcijski linijski spektar, svojstven za svaki atom. Kemijska svojstva atoma određena su uglavnom rasporedom elektrona u vanjskim ljuskama. Atomi se međusobno vežu i prenošenjem ili posudbom elektrona stvaraju veće strukture, molekule i kristalne rešetke. Jezgre nekih atoma mijenjaju se spontano, bilo prerazmještajem protona i neutrona bilo promjenom broja protona i neutrona. Tom prilikom atomska jezgra otpušta gama zračenje, odnosno alfa zračenje ili beta zračenje. Takvi se atomi nazivaju radioaktivnima. Svi atomi teži od bizmuta radioaktivni su. Prilikom promjene stvarnoga broja protona i neutrona atom transmutira, odnosno prelazi u atom različitoga kemijskog elementa. Taj se proces naziva radioaktivni raspad.
Povijest[uredi | uredi kôd]
Poznavanje atoma prošlo je kroz dugi povijesni razvoj. Začetci su se javili 400 god. pr. Kr. s atomizmom. Dugo su prevladavale teorije o kontinuiranoj građi tvari, pod utjecajem Aristotela. Tek u 16. i 17. stoljeću atomističke ideje oživljuju Francis Bacon, Isaac Newton, Galileo Galilei. Godine 1750. Ruđer Bošković pretpostavlja da temeljni sastavni dijelovi tvari imaju istu masu u geometrijskoj točki bez dimenzija. Danas je bit te ideje općeprihvaćena.
Veći pomak u razvoju atomske teorije nastao je tek početkom 19. stoljeću s razvojem shvaćanja o kemijskim elementima i povezivanjem tog pojma s postojanjem atoma (John Dalton; Amedeo Avogadro). Gotovo polovica danas poznatih kemijskih elemenata otkrivena je u 19. stoljeću. Godine 1897. otkriven je elektron (Joseph John Thomson) i prvi model atomske strukture. Godine 1911. Ernest Rutherford pokazuje postojanje sićušne i teške jezgre atoma u pokusima s alfa-česticama. U atomskoj spektroskopiji linijski atomski spektri omogućili su proučavanje strukture elektronskog omotača. Godine 1913. Niels Bohr pretpostavlja kvantizaciju energetskih stanja elektrona u elektronskom omotaču, a 1924. Louis de Broglie pretpostavlja da elektroni imaju valna svojstva (dualizam). Proučavanje razmještaja elektrona u atomu završeno je 1928. prinosima Erwina Schrödingera, Wolfganga Paulija, Maxa Borna i Wernera Heisenberga. Godine 1932. James Chadwick otkrio je neutron. Slijedi brz razvoj nuklearne fizike. S razvojem akceleratora čestica 1960-ih otkriveno je mnoštvo elementarnih čestica.
Modeli atoma[uredi | uredi kôd]
- Prvi model atoma pripisuje se Demokritu. Pošto u to doba nije bilo nikakvih saznanja o strukturi atoma (nisu postojali elektronski mikroskopi), atomi su zamišljani kao jako malene nedjeljive kuglice.
- Thomsonov model atoma ili model pudinga sa šljivama: kad je otkriven elektron, stvorena je teorija da su u središtu atoma elektroni, a svuda okolo je pozitivan električni naboj. Usporedba je grožđica u pudingu (grožđice su malene, a zdjelica pudinga velika).
- Rutherfordov model atoma ili planetarni model atoma je model atoma prema kojem se atom svakog kemijskog elementa u neutralnom stanju sastoji od električno pozitivne atomske jezgre u kojoj je skoncentrirana gotova sva masa atoma i određenog broja elektrona koji se okreću oko atomske jezgre i čine omotač atoma. Ukupni negativni električni naboj elektrona jednak je pozitivnom električnom naboju atomske jezgre i zato je atom prema okolini neutralan.[3]
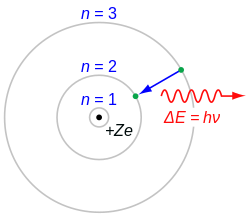
- Bohrov model atoma je ustanovljen poslije Rutherfordovih pokusa kojima je utvrđeno da je u centru atoma malena pozitivno nabijena jezgra (nucleus), a elektroni kruže u orbitale oko jezgre poput planeta koji kruže oko Sunca. No, da bi model bio prihvaćen, trebalo je riješiti sljedeći problem: jezgra je pozitivno nabijena, elektron negativno, zašto elektron uopće kruži oko jezgre, zašto se ne spoji s jezgrom? Rješenje je prodložio 1913. godne Niels Bohr sa sljedeće 4 pretpostavke:
- 1. Elektroni postoje u orbitalama koje posjeduju diskretne (kvantizirane) energije. To znači da ne postoji kontinuirani mogući razmak između jezgre i orbitale, nego su mogući samo neki razmaci. Ti razmaci i njima odgovarajuće energije ovise o konkretnom atomu koga razmatramo.
- 2. Zakoni klasične mehanike ne vrijede pri prelasku elektrona iz jedne orbitale u drugu.
- 3. Kad elektron prijeđe iz jedne orbitale u drugu energetska razlika se oslobađa (ili dobiva) u vidu kvanta svjetlosti (kojeg nazivamo foton) čija frekvencija direktno ovisi o energetskoj razlici između dvije orbite.
- gdje je f frekvencija fotona, E energetska razlika, a h je konstanta poznata kao Planckova konstanta. Ako definiramo da je možemo pisati
- gdje je ω kutna frekvencija fotona.
- 4. Dozvoljene orbitale ovise o kvantiziranim (diskretnim) vrijednostima kutnog momenta L prema jednadžbi:
- Gdje je n = 1,2,3,… i zovemo ga kvantni broj kutnog momenta.
- 4. Današnji model atoma nazivamo kvantno-mehanički model, jer je s vremenom utvrđeno da Bohrov model ne odgovara baš najbolje pokusima, da elektroni ne kruže baš po kružnicama, nego slike dostupne pomoću elektronskih mikroskopa prikazuju nam elektronske oblake.
Podjela atomske fizike[uredi | uredi kôd]
Proučavanjem atoma bavi se više grana moderne fizike. Strukturu elektronskog omotača i međudjelovanje atoma proučava atomska i molekularna fizika. Jezgru atoma proučava nuklearna fizika, subatomske čestice (protone, neutrone i drugo) fizika elementarnih čestica. Atomima se danas upravlja (manipulira) na različite načine. Moguće im je potpuno skinuti elektronski omotač bombardiranjem elektronima u ionskim stupicama (teški ioni) i zatim na metalnim površinama napuniti samo vanjske ljuske, a time se stvara šuplji atom, kao poseban izvor rendgenskoga zračenja.
Atom se iskorištava za proučavanje međudjelovanja i veličine elementarnih čestica, zamjenom bilo elektrona bilo jezgre nekom odgovarajućom nabijenom česticom. Na primjer mioni, π-mezoni ili antiprotoni mogu zamijeniti elektron, a pozitron može zamijeniti jezgru. Tada se govori o egzotičnim atomima.
Moguće ih je ohladiti do temperature mikrokelvina u atomskim stupicama i upotrebljavati za najpreciznija mjerenja (atomski sat), snimiti kako se šeću po površinama pretražnim mikroskopom s tuneliranjem; graditi različite strukture od pojedinačnih atoma nanostrukture; manipulirati atomima kao što se manipulira svjetlošću (atomska optika), i tako dalje.
Korištenjem valnih svojstava atoma razvija se, analogno optičkoj interferometriji, atomska interferometrija kao tehnika dosad najpreciznijih mjerenja u fizici. Ostvarenje Bose-Einsteinove kondenzacije u razrijeđenim parama omogućava stvaranje koherentnih snopova atoma (atomski laser).
Etimologija[uredi | uredi kôd]
Riječ atom dolazi od starogrčke riječi atomos - nedjeljiv, što je u skladu s vjerovanjem (aktualnim do 19. stoljeća) da su atomi najmanji djeljivi elementi materije.
Izvori[uredi | uredi kôd]
Literatura[uredi | uredi kôd]
- Ivan Filipović, Stjepan Lipanović: Opća i anorganska kemija, Školska knjiga, Zagreb, 1995.
Vanjske poveznice[uredi | uredi kôd]
| Zajednički poslužitelj ima stranicu o temi Atom | |
| Zajednički poslužitelj ima još gradiva o temi Atom | |
| Wječnik ima rječničku natuknicu atom |
- Povijest fizike Filozofski fakultet u Rijeci
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||




