Izotop




Izotop (grč. isos: isti, topos: mjesto) je atom istoga kemijskog elementa (isti atomski broj Z) koji se međusobno razlikuje po broju neutrona u atomskoj jezgri, pa prema tome i po masenome broju, odnosno masi. Izotopi nekoga kemijskog elementa zauzimaju isto mjesto u periodnom sustavu, pa im odatle ime, koje im je nadjenuo F. Soddy. Pojedini izotopi označuju se pripadajućim masenim brojem, koji se kao superskript stavlja uz simbol elementa, na primjer izotopi klora su 35Cl (75% u prirodnom elementu) i 37Cl (25%). Naziv izotopi odnosi se, dakle, na različite vrste atoma samo jednog određenog kemijskog elementa, ali se on često neprecizno koristi za skup koji obuhvaća izotope različitih elemenata, na primjer za sve one koji se upotrebljavaju u medicini. Međutim, atomi različitih elemenata ne mogu biti međusobno izotopni i u takvim ih je slučajevima ispravnije nazivati zajedničkim nazivom nuklidi.[1]
Izotopi mogu biti:
- stabilni i
- nestabilni (radionuklidi ili radioizotopi)
Stabilnost, odnosno nestabilnost jezgre je uvjetovana omjerom protona i neutrona. Ako je omjer optimalan, jezgra je stabilna. Na primjer jezgra s 2 protona i 2 neutrona je stabilna jezgra. Budući da se protoni međusobno odbijaju dodaju se neutroni za ravnotežu.
Budući da izotopi imaju jednak broj protona, pa prema tome i jednak broj elektrona u elektronskom omotaču, njihova svojstva i svojstva njihovih spojeva vrlo su slična, a minimalne razlike (izotopni učinci) proizlaze iz različitih atomskih masa. To su razlike u gustoći, viskoznosti, indeksu loma, toplinskoj provodnosti, toplinama isparavanja i taljenja te drugim svojstvima spojeva. Najveće se razlike opažaju između izotopa lakih elemenata, gdje su razlike u atomskim masama najveće, kao na primjer između vodikovih izotopa 1H i 2H (deuterij). Kemijska reakcija, koja kao rezultat ima samo preraspodjelu izotopa nekog elementa među reagirajućim tvarima, naziva se izotopnom izmjenom, na primjer:
- 14 NH4+ + 15 NH3 = 15 NH4 + 14 NH3
Stabilni izotopi[uredi | uredi kôd]
Većina kemijskih elemenata u prirodi smjese su prirodnih izotopa, koji su bilo stabilni bilo radioaktivni (nestabilni). Stabilne izotope ima 81 kemijski element. To su redom svi elementi, od vodika (Z = 1) do uključivo bizmuta (Z = 83), uz iznimku tehnecija (Z = 43) i prometija (Z = 61). Mnogi elementi imaju više stabilnih izotopa, a to je razlogom što njihove relativne atomske mase nisu cijeli brojevi. Vodik je, na primjer, smjesa stabilnih izotopa 1H i 2H, ugljik sadrži stabilne izotope 12C i 13C, kisik izotope 16O, 17O i 18O i tako dalje. Najviše stabilnih izotopa, njih 10, ima kositar. Ukupno se u prirodi nalazi oko 270 vrsta stabilnih i oko 70 vrsta radioaktivnih nuklida.
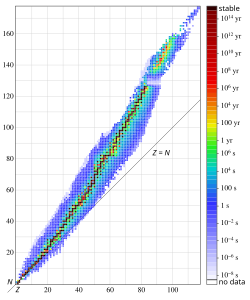
Radioaktivni izotopi, radioizotopi (radionuklidi) pojedinih elemenata, podrijetlom su prirodni ili umjetni. Prirodne radioizotope imaju mnogi elementi koji sadrže i stabilne izotope, a također i svi prirodni radioaktivni elementi, to jest oni koji ne sadrže stabilne izotope. To su elementi od polonija do uključivo plutonija (Z = 84 do 94) te element prometij. Nuklearnim reakcijama mogu se proizvesti umjetni radioizotopi gotovo svih elemenata, pa je danas poznato oko 2 500 vrsta nuklida, što prirodnih, što umjetnih. Svi se oni mogu svrstati u kartu nuklida, u kojoj je svaki nuklid prikazan kvadratom s različitim, za njega karakterističnim podatcima (izotopna obilnost, vrijeme poluraspada, vrsta i energija zračenja i tako dalje). Izotopi pojedinih elemenata svrstani su u vodoravnim redovima prema rastućoj masi.
Nestabilni izotopi[uredi | uredi kôd]
Nestabilni izotopi, odnosno radioaktivni izotopi ili radionuklidi su atomi koji imaju omjer protona i neutrona veći ili manji od omjera potrebnog za stabilnost. Nestabilni izotopi teže stabilnosti, a to se postiže radioaktivnim raspadom (radioaktivnost). Posljedice radioaktivnog raspada je mijenjanje mase i/ili kemijskih svojstava radionuklida uz istodobno emitiranje ionizirajućeg zračenja. Svi elementi iznad rednog broja 82 (olovo) su nestabilni jer odbojnim silama protona više nisu dovoljni neutroni kao ravnoteža. Naime, prevelika je koncentracija protona na jednom mjestu.
Jezgra radionuklida se spontano raspada prelazeći pri tome u neku drugu jezgru. Prilikom raspada jezgra radionuklida emitira čestice i /ili elektromagnetske zrake kratke valne duljine. Emitirane čestice i elektromagnetske zrake se jednim imenom zovu ionizirajuće zračenje. To je pojava radioaktivnosti, a sam proces je transmutacija, tj. spontani prijelaz jedne jezgre u drugu, što se naziva radioaktivni raspad.
Nuklid je atom kemijskog elementa za koji je točno poznat ne samo redni ili atomski broj Z, već i ukupan broj nukleona (protona i neutrona) u atomskoj jezgri. U prirodi postoji samo 92 kemijska elementa i još 12 umjetno proizvedenih, a poznato je oko 3 100 različitih nuklida, od kojih je 350 prirodnih i 2 750 umjetnih. Većina nuklida je nestabilna (radioaktivna), oko 2800. Pogodna kombinacija protona i neutrona čini atomsku jezgru stabilnom, čim je drugačije jezgra se nastoji izbacivanjem nukleona približiti stabilnoj konfiguraciji. Energijske razine u jezgri se popunjavaju kako bi se dostigla konfiguracije minimalne energije, to jest maksimalne stabilnosti.
Povijest[uredi | uredi kôd]
Frederick Soddy je uveo pojam izotopa 1913., kao različitog atoma istog kemijskog elementa, kojem atomska jezgra ima jednaki električni naboj, a različitu atomsku masu. Izotopi (grč. isos - isti, topos - mjesto) upućuje se na činjenicu da su smješteni na istom mjestu u periodnom sustavu elemenata, su atomi istog kemijskog elementa koji imaju isti broj protona i elektrona, a različit broj neutrona, zbog čega imaju ista kemijska svojstva, ali različitu atomsku masu.
Joseph John Thomson je potvrdio postojanje izotopa svojim pokusima 1913. U početku se mislilo da postoje samo radioaktivni izotopi, ali Thomson je dokazao da izotope imaju i stabilni elementi. On je istražujući svojstva teških iona i atomskih jezgri, koji su prolazili kroz kombinirano električno i magnetsko polje, postigao da pomoću tragova na fotografskoj ploči, dobije jasne tragove razdvojenih iona, prema veličini svojih masa. Na osnovu zacrnjenosti tragova dobivenih na fotografskoj ploči, Thomson je utvrdio da kemijski element neon ima dva izotopa atomske mase 20 i 22, koji su kod standardnih uvjeta izmiješani u omjeru 9:1. Kasnije je utvrđeno da neon ustvari ima tri svoja izotopa.
Francis William Aston, engleski fizičar i kemičar, je otkrio 213 stabilnih izotopa kemijskih elemenata. Konstruirao je maseni spektrograf, s pomoću kojega je određivao masu i defekt mase u velikom broju izotopa. Za radove na području istraživanja izotopa dobio je Nobelovu nagradu za kemiju 1922. Treba imati u vidu da se pomoću masene spektrometrije određuju samo relativne vrijednosti atomskih masa. Zato je bilo potrebno da se neka određena masa uzme kao osnova ili standard za uspoređivanje. Za osnovu se uzimala atomska masa kisikovog izotopa kisik-16.
Arthur Jeffrey Dempster je usavršio maseni spektrometar, koji se i naziva Dempsterov maseni spektrometar, a on je imao dvostruko žarište. On je uspio s odgovarajućim kombinacijama električnog i magnetskog polja, koja istovremeno daju fokusiranje po brzini i po pravcu, poboljšati oštrinu linija na fotografskoj ploči. Ovim uređajem Dempster je uspio razdvojiti ione, čije se mase razlikuju samo za 1/4000 atomskih jedinica mase. Uspio je proučavati i teške metale kao što su platina, zlato i uranij, a poznat je po tome što je otkrio izotop uranij-235, osnovni izotop za dobivanje nuklearne fuzije u nuklearnim reaktorima.
Atomska teorija[uredi | uredi kôd]
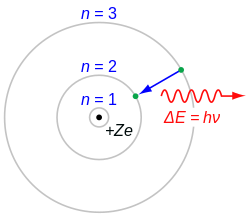
U atomskoj teoriji materije, atom se sastoji od atomske jezgre oko koje kruže elektroni. Danas je općenito priznato mišljenje da se atomska jezgra svih kemijskih elemenata sastoji od pozitivno nabijenih protona i neutrona koji nemaju električni naboj. Čestice koje se nalaze u atomskoj jezgri, to jest protoni i neutroni, zovu se zajedničkim imenom nukleoni (lat. nucleus: jezgra). Neutron ima masu gotovo jednaku masi protona. Proton je jezgra vodikovog atoma, pa mu je masa jednaka masi atoma vodika. Broj protona u atomskoj jezgri koji se zove atomski broj, jednak je njezinom električnom naboju i uvijek odgovara rednom broju kemijskog elementa u periodnom sustavu. Dakle atomskim brojem određena je vrsta kemijskog elementa.
U neutralnom atomu broj elektrona što kruže oko jezgre jednak je broju protona u jezgri. Pozitivan naboj jednog protona jednako je velik kao negativan naboj elektrona. 1869. ruski kemičar D. I. Mendeljejev otkrio je zakonitost ponavljanja kemijskih svojstva elemenata kod povećanja njihove atomske mase. On je tada sve poznate elemente poredao po rastućim atomskim masama jedan iznad drugoga i sastavio periodičku tablicu. Mendeljejev je dokazao da svaki kemijski element ima određen sastav atoma koji označuje atomska masa i mjesto u periodnom sustavu elemenata.
Broj protona P i neutrona N u jezgri određuje atomsku masu A određenog elementa, to jest:
i zove se maseni broj atoma. Na primjer jezgra helija sastoji se od dva protona i dva neutrona. Prema tome je električni naboj jezgre i redni broj helija 2, a relativna atomska masa 4. Oko atomske jezgre kruže negativno nabijeni elektroni, a broj elektrona jednak je broju protona u jezgri.
No kod istog broja protona u jezgri mogu postojati različite količine neutrona. Dva atoma koji imaju isti broj protona, a različiti broj neutrona, imaju skoro ista kemijska svojstva i isti redni broj, ali različite atomske mase. Takvi se elementi koji imaju isti redni broj, a različitu atomsku masu, zovu izotopi. Tako na primjer postoji klor koji ima redni broj 17, to jest njegova jezgra sadrži 17 protona, dok mu je atomska masa 35, što znači da jezgra njegova atoma sadrži 18 neutrona (17 + 18 = 35). Međutim, postoji i klor s atomskom masom 37, to jest jezgra njegova atoma sadrži 20 neutrona (17 + 20 = 37). Običan klor koji se nalazi u spojevima u prirodi ima atomsku masu 35,46, što znači da je on smjesa tih dvaju izotopa koji su u njemu zastupani u omjeru 3 : 1, to jest:
Prvi izotop klora pišemo simbolički 17Cl35, a drugi 17Cl37. Gornji broj uz kemijski simbol elementa znači relativnu atomsku masu tog elementa, a donji - broj protona u jezgri tog elementa, odnosno njegov redni broj. I vodik ima svoje izotope: 1H1 obični vodik, 1H2 teški vodik ili deuterij i 1H3 tricij.
Ovakvi izotopi nađeni su gotovo kod svih kemijskih elemenata. Tako uranij, koji je najvažniji u dobivanju nuklearne energije, ima 5 izotopa. Uranij ima redni broj 92, a njegovi izotopi imaju atomske mase 234, 235, 237, 238 i 239. U prirodnom uraniju najjače je zastupljen izotop s atomskom masom 238. Ima ga 137 puta više nego izotopa s atomskom masom 235. Ostalih njegovih izotopa ima još i manje. Izotopi se danas vrlo mnogo primjenjuju u medicini, tehnici i privredi, a naročito su veoma važni u proizvodnji nuklearne energije. Odjeljivanje izotopa vrši se centrifugiranjem, destilacijom, difuzijom i tako dalje.
Da se jezgra atoma koja se sastoji od pozitivno nabijenih protona ne razleti, jer se istoimeni električni naboji međusobno odbijaju, uzrok su privlačne sile koje vladaju, između protona i neutrona. To su takozvane sile jezgre ili osnovne sile koje, iako su vrlo velike, djeluju samo na vrlo male daljine, to jest u dimenzijama atomske jezgre. Tumačenje tih sila spada danas u glavne probleme atomske fizike.[2]
Proizvodnja izotopa[uredi | uredi kôd]
Odjeljivanje izotopa iz izotopne smjese temelji se na razlikama svojstava, ali je otežano jer su te razlike neznatne. U tu se svrhu primjenjuju molekularno-kinetičke metode (elektroliza, centrifugiranje, difuzija plinova kroz polupropusnu stijenku, frakcijsko taloženje, ionska izmjena, termodifuzija, migracija iona, pobuda laserom i drugo). Na razlikama u specifičnim nabojima iona temelji se elektromagnetska metoda. Za potrebe nuklearne energetike neke su metode odjeljivanja razvijene do industrijskih razmjera, na primjer metoda difuzije za razdvajanje uranijevih izotopa 235U i 238.U. Umjetni radioaktivni izotopi mogu se proizvesti u nuklearnome reaktoru (bombardiranjem atomskih jezgara neutronima ili nuklearnom fisijom teških jezgara) ili pak bombardiranjem nabijenim česticama u akceleratoru čestica.
Primjena izotopa[uredi | uredi kôd]
Primjena izotopa temelji se na njihovim različitim masama i, za radioaktivne izotope, na zračenju koje emitiraju. Kao snažni izvori zračenja izotopi se u radijacijskoj tehnologiji primjenjuju za sterilizaciju i mikrobiološku dekontaminaciju. Značajna je primjena izotopa za izotopno obilježavanje (markiranje), za što su posebno pogodni radioaktivni izotopi, jer se zračenje lako otkriva i mjeri s visokom osjetljivošću. Obilježavanje se sastoji u ugrađivanju takvih izotopa (obilježivač) u fizičke, kemijske i biološke strukture, gdje oni, sudjelujući u reakcijama i procesima, omogućuju praćenje puta pojedinih atoma ili molekula, a time i reakcijskoga mehanizma.
U fizici se izotopi koriste za istraživanja difuzije, kristalizacije, emisije iona te određivanje struktura molekula i kristala. Izotopni učinci u kemiji pružaju informacije o brzini i mehanizmu kemijskih reakcija. Vrlo osjetljive metode omogućuju kvantitativno određivanje iznimno malih količina (tragova) tvari i nekih fizikalno-kemijskih svojstava (topljivost, ravnoteža faza, površinska aktivnost). Zahvaljujući domišljatim primjenama izotopa postignuti su veliki uspjesi u suvremenoj biokemiji i fiziologiji: objašnjena je sinteza ugljikohidrata, bjelančevina i nukleinskih kiselina u živim organizmima i izmijenjena su znanja o fotosintezi. U poljoprivredi se izotopi koriste za praćenje metaboličkih putova u hranidbi biljaka i životinja. Na temelju raspodjele i obilnosti prirodnih izotopa u geološkim formacijama zaključuje se o okolnostima u kojima su nastali pojedini dijelovi Zemljine kore. Starost arheoloških nalaza može se odrediti na temelju količine i vrste nađenih izotopa. Dodavanjem izotopa gorivima, mazivima, talinama i drugom omogućuje se praćenje dinamike procesa u nepristupačnim sredinama (na primjer strujanje plinova u pećima, raspored primjesa u metalurškim pećima, trošenje mehaničkih dijelova i tako dalje). Vrlo je značajna primjena izotopa u medicini. Snažni izvori zračenja, ponajprije kobaltov i cezijev izotop (60Co i 137Cs), služe za radioterapiju, a neki drugi izotopi za vizualizaciju i istraživanje rada organa, lokalizaciju tumora, određivanje metaboličkih putova, ispitivanje djelovanja lijekova i tako dalje. Jedan je od najviše upotrebljavanih izotopa tehnecijev radioaktivni izotop 99mTc.
Broj izotopa po kemijskom elementu[uredi | uredi kôd]
Od 80 kemijskih elemenata, koji imaju stabilne izotope, najviše ih ima kositar i to 10. Ksenon je jedini element koji ima 9 stabilnih izotopa. Četiri elementa ima 7 stabilnih izotopa, devet elemenata ima 6 stabilnih izotopa, devet elemenata ima 5 stabilnih izotopa, devet elemenata ima 4 stabilna izotopa, pet elemenata ima 3 stabilna izotopa, šesnaest elemenata ima 2 stabilna izotopa, te dvadeset i šest elemenata ima samo jedan stabilni izotop (mononuklidni elementi). Ustvari, postoji 19 radionuklidnih elemenata sa samo jednim izotopom, ali su 3 radioaktivna izotopa. Sveukupno ima 255 nuklida koji su stabilni i ne doživljavaju radioaktivni raspad, tako da je u prosjeku (255 / 80 = 3,2) 3,2 stabilnih izotopa po kemijskom elementu.
| Z |
Naziv |
Kemijski simbol |
Atomska masa (g/mol) |
Odabrani izotopi |
|---|---|---|---|---|
| 1 | Vodik | H | 1,00794(7) | Procij (Vodik-1), Deuterij (Vodik-2), Tricij (Vodik-3), (Vodik-4), (Vodik-5) |
| 2 | Helij | He | 4,002602(2) | (teoretska jezgra Helija-2), Helij-3, Helij-4 |
| 3 | Litij | Li | 6,941(2) | Litij-6, Litij-7 |
| 4 | Berilij | Be | 9,012182(3) | Berilij-8, Berilij-9, Berilij-10 |
| 5 | Bor | B | 10,811(7) | Bor-10, Bor-11 |
| 6 | Ugljik | C | 12,0107(8) | Ugljik-11, Carbon-12, Ugljik-13, Ugljik-14 |
| 7 | Dušik | N | 14,0067(2) | Dušik-13, Dušik-14, Dušik-15 |
| 8 | Kisik | O | 15,9994(3) | Kisik-13, Kisik-15, Kisik-16, Kisik-17, Kisik-18 |
| 9 | Fluor | F | 18,9984032(5) | Fluor-17, Fluor-18, Fluor-19 |
| 10 | Neon | Ne | 20,1797(6) | Neon-20, Neon-21, Neon-22 |
| 11 | Natrij | Na | 22,98976928(2) | Natrij-22, Natrij-23 |
| 12 | Magnezij | Mg | 24,3050(6) | Magnezij-23, Magnezij-24, Magnezij-25, Magnezij-26 |
| 13 | Aluminij | Al | 26,9815386(8) | Aluminij-26, Aluminij-27 |
| 14 | Silicij | Si | 28,0855(3) | Silicij-28, Silicij-29, Silicij-30 |
| 15 | Fosfor | P | 30,973762(2) | Fosfor-30, Fosfor-31, Fosfor-32, Fosfor-33 |
| 16 | Sumpor | S | 32,065(5) | Sumpor-32, Sumpor-33, Sumpor-34, Sumpor-36 |
| 17 | Klor | Cl | 35,453(2) | Klor-35, Klor-37 |
| 18 | Argon | Ar | 39,948(1) | Argon-36, Argon-38, Argon-40 |
| 19 | Kalij | K | 39,0983(1) | Kalij-39, (Kalij-40)*, Kalij-41 |
| 20 | Kalcij | Ca | 40,078(4) | Kalcij-40, Kalcij-42, Kalcij-43, Kalcij-44, Kalcij-46, Kalcij-48 |
| 21 | Skandij | Sc | 44,955912(6) | Skandij-45 |
| 22 | Titanij | Ti | 47,867(1) | Titanij-44, Titanij-46, Titanij-47, Titanij-48, Titanij-49, Titanij-50 |
| 23 | Vanadij | V | 50,9415(1) | Vanadij-49, Vanadij-50, Vanadij-51 |
| 24 | Krom | Cr | 51,9961(6) | Krom-50, Krom-52, Krom-53, Krom-54 |
| 25 | Mangan | Mn | 54,938045(5) | Mangan-55 |
| 26 | Željezo | Fe | 55,845(2) | Željezo-52, Željezo-54, Željezo-55, Željezo-56, Željezo-57, Željezo-58, Željezo-60 |
| 27 | Kobalt | Co | 58,933195(5) | Kobalt-56, Kobalt-57, Kobalt-59, Kobalt-60 |
| 28 | Nikal | Ni | 58,6934(2) | Nikal-58, Nikal-60, Nikal-61, Nikal-62, Nikal-64 |
| 29 | Bakar | Cu | 63,546(3) | Bakar-63, Bakar-64, Bakar-65 |
| 30 | Cink | Zn | 65,409(4) | Cink-64, Cink-66, Cink-67, Cink-68, Cink-70 |
| 31 | Galij | Ga | 69,723(1) | Galij-69, Galij-71 |
| 32 | Germanij | Ge | 72,64(1) | Germanij-70, Germanij-72, Germanij-73, Germanij-74, Germanij-76 |
| 33 | Arsen | As | 74,92160(2) | Arsen-75 |
| 34 | Selenij | Se | 78,96(3) | Selenij-72, Selenij-74, Selenij-76, Selenij-78, Selenij-79, Selenij-80, Selenij-82, Selenij-87 |
| 35 | Brom | Br | 79,904(1) | Brom-79, Brom-81 |
| 36 | Kripton | Kr | 83,798(2) | Kripton-78, Kripton-80, Kripton-82, Kripton-83, Kripton-84, Kripton-86 |
| 37 | Rubidij | Rb | 85,4678(3) | Rubidij-85, (Rubidij-87)* |
| 38 | Stroncij | Sr | 87,62(1) | Stroncij-84, Stroncij-86, Stroncij-87, Stroncij-88, Stroncij-90 |
| 39 | Itrij | Y | 88,90585(2) | Itrij-89 |
| 40 | Cirkonij | Zr | 91,224(2) | Cirkonij-90, Cirkonij-91, Cirkonij-92, Cirkonij-93, Cirkonij-94, Cirkonij-96 |
| 41 | Niobij | Nb | 92,906 38(2) | Niobij-93 |
| 42 | Molibden | Mo | 95,94(2) | Molibden-92, Molibden-94, Molibden-95, Molibden-96, Molibden-97, Molibden-98, Molibden-100 |
| 43 | Tehnecij | Tc | [98,9063] | Tehnecij-99, Tehnecij-99m |
| 44 | Rutenij | Ru | 101,07(2) | Rutenij-96, Rutenij-98, Rutenij-99, Rutenij-100, Rutenij-101, Rutenij-102, Rutenij-104, Rutenij-106 |
| 45 | Rodij | Rh | 102,90550(2) | Rodij-103 |
| 46 | Paladij | Pd | 106,42(1) | Paladij-102, Paladij-103, Paladij-104, Paladij-105, Paladij-106, Paladij-107, Paladij-108, Paladij-110 |
| 47 | Srebro | Ag | 107,8682(2) | Srebro-107, Srebro-109 |
| 48 | Kadmij | Cd | 112,411(8) | Kadmij-106, Kadmij-108, Kadmij-110, Kadmij-111, Kadmij-112, Kadmij-113m, Kadmij-114, Kadmij-116 |
| 49 | Indij | In | 114,818(3) | Indij-113, Indij-115 |
| 50 | Kositar | Sn | 118,710(7) | Kositar-112, Kositar-114, Kositar-115, Kositar-116, Kositar-117, Kositar-118, Kositar-119, Kositar-120, Kositar-121m, Kositar-122, Kositar-124, Kositar-126 |
| 51 | Antimon | Sb | 121,760(1) | Antimon-121, Antimon-123 |
| 52 | Telurij | Te | 127,60(3) | Telurij-120, Telurij-122, Telurij-123, Telurij-124, Telurij-125, Telurij-126, Telurij-128, Telurij-130 |
| 53 | Jod | I | 126,90447(3) | (Jod-123)*, (Jod-124)*, (Jod-125)*, Jod-127, (Jod-129)*, (Jod-131)*, (Jod-135)* |
| 54 | Ksenon | Xe | 131,293(6) | Ksenon-124, Ksenon-125, Ksenon-126, Ksenon-128, Ksenon-130, Ksenon-131, Ksenon-132, Ksenon-133, Ksenon-134, Ksenon-135, Ksenon-136 |
| 55 | Cezij | Cs | 132,9054519(2) | Cezij-133, Cezij-134, Cezij-135, Cezij-137 |
| 56 | Barij | Ba | 137,327(7) | Barij-130, Barij-132, Barij-134, Barij-135, Barij-136, Barij-137, Barij-138 |
| 57 | Lantan | La | 138,90547(7) | Lantan-139 |
| 58 | Cerij | Ce | 140,116(1) | Cerij-136, Cerij-138, Cerij-140, Cerij-142 |
| 59 | Praseodimij | Pr | 140,90765(2) | Praseodimij-141 |
| 60 | Neodimij | Nd | 144,242(3) | Neodimij-142, Neodimij-143, Neodimij-144, Neodimij-145, Neodimij-146, Neodimij-148, Neodimij-150 |
| 61 | Prometij | Pm | [146,9151] | Prometij-147 |
| 62 | Samarij | Sm | 150,36(2) | Samarij-144, Samarij-147, Samarij-148, Samarij-149, Samarij-150, Samarij-151, Samarij-152, Samarij-154 |
| 63 | Europij | Eu | 151,964(1) | Europij-151, Europij-153, Europij-155 |
| 64 | Gadolinij | Gd | 157,25(3) | Gadolinij-152, Gadolinij-154, Gadolinij-155, Gadolinij-156, Gadolinij-157, Gadolinij-158, Gadolinij-160 |
| 65 | Terbij | Tb | 158,92535(2) | Terbij-159 |
| 66 | Disprozij | Dy | 162,500(1) | Disprozij-158, Disprozij-160, Disprozij-161, Disprozij-162, Disprozij-163, Disprozij-164 |
| 67 | Holmij | Ho | 164,93032(2) | Holmij-165 |
| 68 | Erbij | Er | 167,259(3) | Erbij-162, Erbij-164, Erbij-166, Erbij-167, Erbij-168, Erbij-170 |
| 69 | Tulij | Tm | 168,93421(2) | Tulij-169 |
| 70 | Iterbij | Yb | 173,04(3) | Iterbij-168, Iterbij-170, Iterbij-171, Iterbij-172, Iterbij-173, Iterbij-174, Iterbij-176 |
| 71 | Lutecij | Lu | 174,967(1) | Lutecij-175, Lutecij-176 |
| 72 | Hafnij | Hf | 178,49(2) | Hafnij-174, Hafnij-176, Hafnij-177, Hafnij-178, Hafnij-179, Hafnij-180 |
| 73 | Tantal | Ta | 180,9479(1) | Tantal-181 |
| 74 | Volfram | W | 183,84(1) | Volfram-180, Volfram-182, Volfram-183, Volfram-184, Volfram-186 |
| 75 | Renij | Re | 186,207(1) | Renij-185, Renij-187 |
| 76 | Osmij | Os | 190,23(3) | Osmij-184, Osmij-186, Osmij-187, Osmij-188, Osmij-189, Osmij-190, Osmij-192 |
| 77 | Iridij | Ir | 192,217(3) | Iridij-191, Iridij-192, Iridij-193 |
| 78 | Platina | Pt | 195,084(9) | Platina-192, Platina-194, Platina-195, Platina-196, Platina-198 |
| 79 | Zlato | Au | 196,966569(4) | Zlato-197 |
| 80 | Živa | Hg | 200,59(2) | Živa-196, Živa-198, Živa-199, Živa-200, Živa-201, Živa-202, Živa-204 |
| 81 | Talij | Tl | 204,3833(2) | Talij-203, Talij-205, (Talij-207)*, (Talij-208)*, (Talij-210)* |
| 82 | Olovo | Pb | 207,2(1) | Olovo-204, Olovo-206, Olovo-207, Olovo-208, Olovo-209, (Olovo-210)*, (Olovo-211)*, (Olovo-212)*, (Olovo-214)* |
| 83 | Bizmut | Bi | 208,98040(1) | Bizmut-209, (Bizmut-210)*, (Bizmut-211)*, (Bizmut-212)*, (Bizmut-214)* |
| 84 | Polonij | Po | [208,9824] | Polonij-210, (Polonij-211)*, (Polonij-212)*, (Polonij-214)*, (Polonij-215), (Polonij-216)*, (Polonij-218)* |
| 85 | Astat | At | [209,9871] | Astat-211 |
| 86 | Radon | Rn | [222,0176] | (Radon-219)*, (Radon-220)*, (Radon-222)* |
| 87 | Francij | Fr | [223,0197] | (Francij-223)* |
| 88 | Radij | Ra | [226,0254] | (Radij-223)*, (Radij-224)*, (Radij-226)*, (Radij-227)*, (Radij-228)* |
| 89 | Aktinij | Ac | [227,0278] | (Aktinij-222)*, (Aktinij-223)*, (Aktinij-224)*, (Aktinij-225)*, (Aktinij-226), (Aktinij-227)* |
| 90 | Torij | Th | 232,03806(2) | (Torij-227)*, (Torij-228)*, (Torij-229)*, (Torij-230)*, (Torij-231)*, (Torij-232)*, (Torij-233)*, (Torij-234)* |
| 91 | Protaktinij | Pa | 231,03588(2) | (Protaktinij-230)*, (Protaktinij-231)*, (Protaktinij-234) |
| 92 | Uranij | U | 238,02891(3) | (Uranij-230)*, (Uranij-231)*, (Uranij-232)*, (Uranij-233)*, (Uranij-234)*, (Uranij-235)*, (Uranij-236)*, (Uranij-238)*, (Uranij-239)* |
| 93 | Neptunij | Np | [237,0482] | (Neptunij-235)*, (Neptunij-236)* |
| 94 | Plutonij | Pu | [244,0642] | (Plutonij-238)*, (Plutonij-239)*, (Plutonij-240)*, (Plutonij-241)*, (Plutonij-242)*, (Plutonij-244)* |
| 95 | Americij | Am | [243,0614] | (Americij-241)*, (Americij-242)*, (Americij-243)* |
| 96 | Kurij | Cm | [247,0703] | |
| 97 | Berkelij | Bk | [247,0703] | |
| 98 | Kalifornij | Cf | [251,0796] | |
| 99 | Einsteinij | Es | [252,0829] | |
| 100 | Fermij | Fm | [257,0951] | |
| 101 | Mendelevij | Md | [258,0986] | |
| 102 | Nobelij | No | [259,1009] | |
| 103 | Lorensij | Lr | [260,1053] | |
| 104 | Rutherfordij | Rf | [261,1087] | |
| 105 | Dubnij | Db | [262,1138] | |
| 106 | Seaborgij | Sg | [263,1182] | |
| 107 | Bohrij | Bh | [262,1229] | |
| 108 | Hassij | Hs | [265] | |
| 109 | Meitnerij | Mt | [266] | |
| 110 | Darmstadij | Ds | [269] | |
| 111 | Roentgenij | Rg | [272] | |
| 112 | Kopernicij | Cn | [285] | |
| 113 | Nihonij | Nh | [284] | |
| 114 | Flerovij | Fl | [289] | |
| 115 | Moskovij | Mc | [288] | |
| 116 | [[Livermorij] | Lv | [292] | |
| 117 | Tenesin | Ts | [295] | |
| 118 | Oganeson | Og | [294] |
Izvori[uredi | uredi kôd]
- Ivan Filipović, Stjepan Lipanović: Opća i anorganska kemija, Školska knjiga, Zagreb, 1995.


