Torij
| torij | ||
|---|---|---|
|
| ||
| Osnovna svojstva | ||
Element Simbol Atomski broj |
torij Th 90 | |
| Kemijska skupina | aktinoidi | |
| Grupa, perioda, Blok | Ac, 7, f | |
| Izgled | sivi prah | |
| Gustoća1 | 11700 kg/m3 | |
| Tvrdoća | 3,0 po Mohsovoj ljestvici | |
| Specifični toplinski kapacitet (cp ili cV)2 |
26,23 J mol–1 K–1 | |
| Talište | 1842 °C | |
| Vrelište3 | 4788[1] °C | |
| Toplina taljenja | 13,81 kJ mol-1 | |
| Toplina isparavanja | 514 kJ mol-1 | |
|
1 pri standardnom tlaku i temperaturi | ||
| Atomska svojstva | ||
| Atomska masa | 232,03806(2) | |
| Elektronska konfiguracija | [Rn] 6d27s2[1] | |
Torij je kemijski element atomskog (rednog) broja 90 i atomske mase 232,03806(2). U periodnom sustavu elemenata predstavlja ga simbol Th. Torij je radioaktivan kemijski element iz skupine aktinoida, a u prirodi se torij nalazi kao smjesa 12 radioaktivnih izotopa, od kojih je najstabilniji torij-232, s vremenom poluraspada od 1,4 x 1010 godina, dva su srednje dugog vremena poluraspada (torij-229 - 7900 godina i torij-230 - 75400 godina), a svi ostali su kratkoživući izotopi (uključujući i trinaest umjetno dobivenih izotopa). Izotop torij-232 je emiter alfa-čestica, koji prirodnim raspadnim nizom torija prolazi kroz 6 alfa raspada i 4 beta raspada, do konačnog stabilnog izotopa olova-208. U procesu raspada stvara se i plinoviti radon-220 (toron), koji je također jak alfa-emiter, a time i radiotoksičan. Stoga je prostore u kojima je torij (i njegovi spojevi) uskladišten potrebno stalno ventilirati. Izotop torij-232 također je dobar apsorber sporih neutrona koji nizom radioaktivnih pretvorbi stvara uranijev fisilni izotop uranij-233, koji se može koristiti kao nuklearno gorivo.
Povijest[uredi | uredi kôd]
Torij je otkrio šveđanin Jöns Jakob Berzelius 1828. i dao mu ime po skandinavskom bogu rata Toru.
Zalihe i izvori[uredi | uredi kôd]
Procjenjuje se da je u sastavu Zemljine kore torij zastupljen 3 puta više od uranija i podjednako kao olovo ili molibden.
Najpoznatiji minerali u kojima se nalazi su: torit (ThO2), torijanit (ThO2 + UO2) i monacit, koji uz minerale većine rijetkih zamalja sadrži i 3 - 9% ThO2. Nalazišta monacitnog pijeska su u Brazilu, južnoj Indiji, Šri Lanki i SAD-u. Velika nalazišta torijevih minerala, koja se još ne koriste, nalaze se u SAD-u (Nova Engleska).[2]
Svojstva[uredi | uredi kôd]




U čistom elementarnom stanju torij je sivi prah ili poput platine siv, dosta mekan i rastezljiv metal.
Relativno je postojan na zraku, tako da sjaj gubi tek nakon nekoliko mjeseci. Međutim, ako je onečišćen oksidom znatno brže potamni, pa preko sive prelazi u potpuno crnu boju. Fizikalna svojstva bitno ovise o količini sadržanih nečistoća, tako da i "čisti" torij sadrži više desetinki postotka oksida.
Otporan je prema razrijeđenim kiselinama, topljiv u dimljivoj klorovodičnoj kiselini i u zlatotopci.
S vodikom reagira na srednje povišenim temperaturama stvarajući dva hidrida ThH2 pseudotetragonske strukture i ThH4 kubične strukture, nevezane s originalnom torijevom kristalnom strukturom.
Dobivanje torija[uredi | uredi kôd]
Glavne rude u kojima ima torija su torijanit, monacit; također je u velikim količinama nazočan u cirkoniju, titanitu, gadolinitu i betafitu. Komercijalno se dobiva iz monacitnog pijeska, u kojem ima puno elemenata rijetkih zemalja (cerij, neodimij, samarij, gadolinij).
Postupak je sljedeći: pijesak se raščini pomoću vruće koncentrirane sumporne kiseline, dobivena otopina sulfata ohladi se do O °C i istaloži oksalnom kiselinom. Za razliku od oksalata rijetkih zemalja, oksalat torija može se kompleksno otopiti u toploj zasićenoj otopini amonijevog oksalata, pa se tako izdvaja, a taloži se ponovnim zakiseljavanjem otopine. Metalni torij može se dobiti redukcijom torijevog oksida kalcijem, elektrolizom anhidrida torijevog klorida u talini natrijevog klorida i kalijevog klorida, te redukcijom torijevog tetraklorida alkalijskim metalima. Svjetska proizvodnja je oko 31 000 m3 na godinu. Smatra se da su rezerve oko 3,3 x 106 tona.
Primjena torija[uredi | uredi kôd]
Torij se uglavnom koristi kao nuklearno gorivo, otkako se utvrdilo da svojim raspadom stvara novo gorivo, izotop uranija-233. Pretpostavlja se da su energetske zalihe torija veće od sveukupnih zaliha fosilnih goriva i uranija.
Služi kao dodatak legurama za grijače električnih otpornih peći, kao sredstvo za apsorpciju plinova u tehnici visokih vakuuma. Radioaktivnim raspadom daje mezotorij, radiotorij, torij X, torijsku emanaciju, torij A, B, C i D i konačno, izotop olovo-208. Torij X, izotop kratka vijeka, služi kao lijek za neke kožne bolesti.
Spojevi torija[uredi | uredi kôd]
Torij stvara kemijske spojeve s oksidacijskim brojem +4, a smatra se da može imati i oksidacijske brojeve +3 i +2. Najvažniji spoj torija je torijev(IV) oksid (ThO2), koji nastaje žarenjem torijeva hidroksida ili soli (npr. torijeva nitrata). To je oksid s najvišim poznatim talištem od 3300 °C. Ovaj oksid koristi se kao legirajući dodatak nekim metalima: volframu (gdje kontrolira rast kristalnih zrna), niklu (očvršćuje kristalnu strukturu) i magneziju, te kao nanos na žarenim volframovim elektrodama jer lako otpušta elektrone. Koristi se i kao efikasan dezoksidans kod dobivanja metala (željeza i molibdena).
Čisti oksid sinteriran iz praha proziran je i ima velik indeks loma, ali malu disperzivnost, pa služi za izradu leća znanstvenih instrumenata. U istu svrhu dodaje se standardnom staklu da mu poboljša optička svojstva. U kombinaciji s malim dodacima cerija služi za punjenje plinskih prenosivih svjetiljki koje, pod djelovanjem slabog plamena, daju blještavu danju svjetlost. Također se koristi kao katalizator pri dobivanju dušične kiseline iz amonijaka, sumporne kiseline, te za krekiranje nafte.
Biološka uloga[uredi | uredi kôd]
Torij nema biološku ulogu, a njegova radiotoksičnost uglavnom prelazi druge oblike toksičnosti.
Smrtonosna doza torijevog(IV) nitrata (oralno, miš) je 1760 mg/kg. Torijevi spojevi su umjereno otrovni (toksični); akutna izloženost može dovesti do dermatitisa, a kronična izloženost izaziva rak.
Torijski nuklearni reaktor[uredi | uredi kôd]
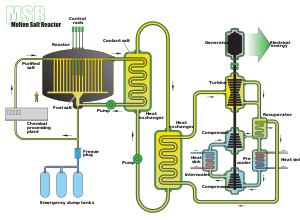
Torijski nuklearni reaktor s tekućim torijevim fluoridom temeljito se razlikuje od većine današnjih nuklearnih reaktora. Jedna tona torija dovoljna je za proizvodnju jednake količine energije kao od 200 tona uranija, što automatski znači i manje radioaktivnog otpada. Nakon iskorištavanja, nastali je otpad opasan samo oko 300 godina, za razliku od današnjeg nuklearnog otpada, koji će biti opasan još bar 10 000 godina. Štoviše, torijski reaktor može iskoristiti otpad uranijskog reaktora za rad. Torij je jeftiniji i može se pakirati u mnogo manje dimenzije. Prema procjenema, Amerika ima oko 440 000 tona torija, Australija i Indija oko 300 000 tona, a Kanada još 100 000 tona. U Americi i Australiji donedavno je odlagan kao otpad.
Torijski je reaktor, reaktor s tekućim torijevim fluoridom ili LFTR (engl. Liquid Fluoride Thorium Reactor), vrlo siguran zahvaljujući svojoj sposobnosti da se ugasi sam od sebe, prije nego dođe do opasnog porasta temperature. LFTR koncept koristi torij i uranij-233 pomiješane sa solima litija i berilija. Tekućina u jezgri nije pod tlakom, a svako povišenje temperature smanjuje snagu rada reaktora, što ga stabilizira i bez potrebe za intervencijom od strane osoblja.
| H | He | ||||||||||||||||||||||||||||||
| Li | Be | B | C | N | O | F | Ne | ||||||||||||||||||||||||
| Na | Mg | Al | Si | P | S | Cl | Ar | ||||||||||||||||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | As | Br | Kr | ||||||||||||||||
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Te | I | Xe | |||||||||||||||
| Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Rn | ||
| Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| Alkalijski metali | Zemnoalkalijski metali | Lantanoidi | Aktinoidi | Prijelazni metali | Slabi metali | Polumetali | Nemetali | Halogeni elementi | Plemeniti plinovi |



