Hans Georg Dehmelt
| Hans Georg Dehmelt | |
| Rođenje | 9. rujna 1922. Görlitz, Saska, Njemačka |
|---|---|
| Prebivalište | SAD |
| Državljanstvo | Nijemac |
| Polje | Fizika |
| Institucija | Sveučilište Washington u Seattleu Sveučilište Duke |
| Alma mater | Sveučilište u Göttingenu |
| Poznat po | Ionska stupica |
| Istaknute nagrade | Nobelova nagrada za fiziku (1989.) |
| Portal o životopisima | |
Hans Georg Dehmelt (Görlitz, 9. rujna 1922.), američki fizičar njemačkoga podrijetla. Diplomirao (1948.) i doktorirao (1950.) na Sveučilištu u Göttingenu. Profesor Sveučilišta Washington u Seattleu, zaslužan za mjerenje magnetizma elektrona s točnošću od dvanaest znamenki. Izmjerena vrijednost magnetskoga dipolnog momenta elektrona (dipol) 1,001 159 652 193(10), gdje posljednje dvije znamenke u zagradi izriču neodređenost mjerenja zadnjih decimalnih mjesta, u nevjerojatnom je suglasju s vrijednošću 1,001 159 652 14 koju predviđa kvantna elektrodinamika. Za razvoj tehnike ionskih stupica podijelio je s W. Paulom i N. F. Ramseyem Nobelovu nagradu za fiziku (1989.).[1]
Ionska stupica[uredi | uredi kôd]

Ionska stupica je uređaj kojim se ioni mogu zadržati u određenom prostoru unutar elektromagnetskog polja. Vrijeme zadržavanja, prema vrsti i namjeni stupice, može varirati od nekoliko sekundi do više dana. Najvažnija je primjena kao analizatora u masenoj spektrometriji, te kod ionskih pumpi za postizanje visokog i ultravisokog vakuuma do 10–9 Pa.[2]
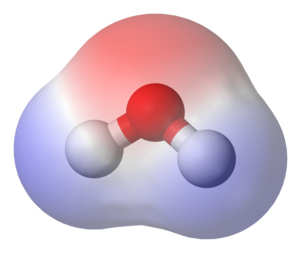
Dipol u kemiji[uredi | uredi kôd]
Dipol, u kemiji, je naziv za nesimetrične molekule, u kojima se, zbog razlike u elektronegativnosti atoma, težišta pozitivnog i negativnog naboja ne poklapaju. Najjednostavniji su primjeri dipola dvoatomne molekule halogenovodika (na primjer HCl) u plinovitu stanju, ali su dipoli i veće molekule kao što su molekule vode, alkohola ili aminokiselina. Sve su to polarne molekule, a veličina njihove polarnosti određena je električnim dipolnim momentom. Polarne molekule plina ili kapljevine zauzimaju u električnom polju određeni položaj prema smjeru polja.[3]
Izvori[uredi | uredi kôd]
- ↑ Dehmelt, Hans Georg, [1] "Hrvatska enciklopedija", Leksikografski zavod Miroslav Krleža, www.enciklopedija.hr, 2015.
- ↑ ionska stupica, [2] "Hrvatska enciklopedija", Leksikografski zavod Miroslav Krleža, www.enciklopedija.hr, 2015.
- ↑ dipol, [3] "Hrvatska enciklopedija", Leksikografski zavod Miroslav Krleža, www.enciklopedija.hr, 2014.
